1.1 DEFINITION OG FOREKOMST
Vejledning for anlæggelse af dræn gennem thoraxvæggen ind i pleurahulen med henblik på at drænere luft, blod, væske eller pus. Vejledningen fokuserer fortrinsvis på håndtering af dræn mindre end 20F.
1.2 ÆTIOLOGI
Anlæggelse af pleuradræn er en essentiel procedure til behandling af mange forskellige tilstande, primært pneumothorax og pleuraeffusion. Pleuradrænage kan være livreddende og nogle tilstande vil udræneret medføre høj mortalitet og morbiditet (1–3). Når proceduren udføres med formål at fjerne væske, kaldes drænanlæggelsen for en pleuracentese.
Pleuradrænage har en lang historie med den tidligst kendte beskrivelse af åben thoraxdrænage af pleuraempyem i Corpus Hippocraticum (4). Drænage med pleuradræn i stedet for åben drænage blev først accepteret som standard of care i 1950’erne og 60’er, hvor også de første plastikkatetre blev markedsført og den moderne vandlås med tre kamre beskrevet (5–7).
I dag findes et bredt udvalg af udstyr og teknikker til pleuradrænanlæggelse. Effektiv billeddiagnostik med røntgen, CT og ultralyd kan hjælpe til afklaring af indikation for pleuradrænanlæggelse (1,8). Ved drænage af væske, pus og blod betragtes ultralydsvejledt drænanlæggelse som obligatorisk, men også ved pneumothoraxdiagnostik og -behandling kan ultralyd benyttes (8–10).
Drænagesystemer med vandlås eller heimlichventil benyttes fortsat, dog er der de seneste år blevet markedsført elektroniske drænsystemer som vinder udbredelse (11).
1.3 INDIKATIONER
- Pneumothorax (se selvstændig DLS-retningslinje)
- Pleuraeffusion (inkl Chylothorax og hydropneumothorax (se selvstændig DLS-retningslinje)
- Empyem og parapneumonisk effusion (se selvstændig DLS-retningelinje)
og (sjældnere i medicinsk regi): - Hæmothorax
- Traumatisk hæmopneumothorax
- Postoperativt (f.eks. Thoracotomi, Hjertekirugi)
1.4 KONTRAINDIKATIONER
Kontraindikationer til anlæggelse af pleuradræn er alle relative, men følgende bør nævnes: koagulopati og antitrombotisk medicin, pleurale bullae, pleurale adherencer, diaphragmaparese og hudinfektion over instiksstedet.
Ved trykpneumothorax: ingen kontraindikationer for livreddende drænanlæggelse.
1.5 FORUNDERSØGELSER
Laboratoriesvar på hæmoglobin, trombocytter og koagulationsfaktorer bør foreligge og ikke være ældre end 7 døgn. Grænseværdier fastlægges i lokal instruks.
Herudover bør der foreligge billeddiagnostik af thorax i form af røntgen, CT og/eller ultralyd mhp. markering af indstiks-sted, som markeres på huden med spritfast tusch eller stumpt markeringsværktøj, såsom hætten fra lokalbedøvelseskanylen.
OBS: Ved klinisk mistanke til trykpneumothorax bør drænanlæggelse ikke afvente billeddiagnostik.
1.6 DRÆN
Der er markedsført en række forskellige dræntyper/systemer, og hvilke som benyttes kan variere fra afdeling til afdeling. Overordnet set kan man skelne imellem ”store” dræn (>14F) og ”små” dræn (≤14F), og om drænet anlægges ved stump dissektion (”kirurgisk teknik”), ved seldinger teknik (over guidewire) eller over trokar (12). Dræn kan være lige eller med ”grisehale” i den distale ende.
Dræn anlagt ved stump dissektion varetages oftest af de kirurgiske specialer og ligger udenfor målet med denne vejledning, men kan benyttes på medicinske afdelinger.
Selvom der findes forskellige systemer og teknikker til anlæggelse af ”små” dræn, vil der oftest være tale om et grisehalekateter anlagt over trokar. Grisehalekatetret består grundlæggende af tre dele, et ydre kateter i blød plast, en hul trokar i metal og inden i denne en solid metalnål. Anlæggelse af grisehalekateter over trokar beskrives under punkt 1.8.
Instruktion i brug af andre dræntyper som f.eks. Tru-Close™, Portex™, dræn anlagt over guidewire eller grisehalekatetre med indlejret snoretræk til at sikre oprulning af drænspidsen bør søges hos producenten.
Drændiameter tilgængelig på en afdeling varierer typisk mellem 6, 10, 12, 16, 20, og eventuelt 28 F.
1F svarer til 0,33mm. Således har et dræn på 6F en ydre diameter på 2mm, et dræn på 12F en ydre diameter på 4mm etc.
Valg af drænstørrelse afhænger af indikationen. Se selvstændige DLS-vejledninger.
1.7 DRÆNPLACERING
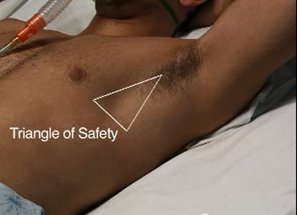
Placeringen af drænet er delvist afhængig af formålet. Ved pneumothorax behandling vil større dræn typisk placeres mellem forreste aksillærlinie, midtaksillærlinien og en horisontal linje gående fra brystvorten (”Den sikre trekant”), således at drænet placeres i 5. intercostalrum. Mindre dræn kan placeres midtklavikulært i 2. intercostalrum. Ved væske (pleuraeffusion, empyem og hæmothorax) er ansamlingens placering afgørende for drænets placering, altid under hensyntagen til a. mammaria interna.
1.8 DRÆNANLÆGGELSE
Anlæggelse af pleuradræn er en risiko-procedure, som kræver informeret samtykke. Der bør altid være en assistent til proceduren.
I særlige tilfælde kan gives anxiolytika forud for proceduren. I så tilfælde gives typisk morfin, fentanyl eller eventuelt benzodiazepin.
Remedier
- Sterile Handsker
- Klorhexidinsprit
- Steril afdækning
- Gaze swabs
- Kanyler (til lokalanalgesi)
- Lidokain 1%-2%, med eller uden adrenalin
- Skalpel eller blad
- Dræn
- Drænplaster eller sutur til fiksering
- Plaster
- 3-vejshane
- Drænpose / drænboks
Lejring
Patienten lejres afhængigt af indikation for pleuradrænanlæggelse og placering af den ansamling som ønskes dræneret.
Ved pneumothorax typisk i rygleje eller sideleje (på den ”raske side”) med hovedgærdet let eleveret. Hvis armen på drænsiden løftes og lægges bag hovedet er der fri adgang til ”den sikre trekant” (se billede). Ved drænplacering i IC2 midtklavikulært holdes begge arme langs siden.
Ved pleuraeffusion kan patienten lejres siddende, gerne med støtte fra ”prædikestol” og evt. fodskammel foran patienten. Svage patienter som ikke kan sidde igennem proceduren kan enten lejres som ved pneumothorax eller alternativt lejres på fladt leje liggende i sideleje hvorefter det apikale lungefelt bliver tilgængeligt for undersøgelse og drænage.
Desinfektion og lokalanæstesi
Incisionsstedet rengøres med klorhexidinsprit. Når klorhexidinen er tørret kan påføres et hulstykke.
Herefter bedøves hud, subkutant væv og det interkostale rum med minimum 5-10ml 1-2% lidocain, gerne med adrenalin, med fokus på at bedøve især hud og pleura. Lokalbedøvelsen lægges langs ribbenets øvre kant for at undgå det neurovaskulære bundt og kan med fordel foregå real-time UL-vejledt. Ved bedøvelse af meget muskuløse eller obese patienter kan der være behov for længere nål og/eller mere lidocain for at opnå sufficient lokalanalgesi. En effektiv lokalbedøvelse slår an efter ca. 3-5 minutter og er kritisk for patientens medvirken og oplevelse af proceduren.
I afslutningen af lokalanæstesi aspireres på sprøjten når nålen er i pleura. Hvis der ikke kan aspireres luft eller væske/pus/blod (afhængig af indikation) er efterfølgende drænanlæggelse kontraindiceret, og der bør igen vurderes med ultralyd.
OBS: Reintroducer ikke aspireret pleuravæske i stikkanalen for at undgå spredning af maligne celler eller bakterier.

Procedure ved anlæggelse af grisehalekateter (< 20F)
Teknikken ved anlæggelse af grisehalekateter i pleura er den samme uanset indikation (13).
- Efter huden er rengjort og bedøvet foretages lille stabincision i huden som passer til drænstørrelsen og følger hudens spaltelinjer.

- Det samlede grisehalekateter indføres langs oversiden af costa, indtil drænet lige netop er inde i pleura.
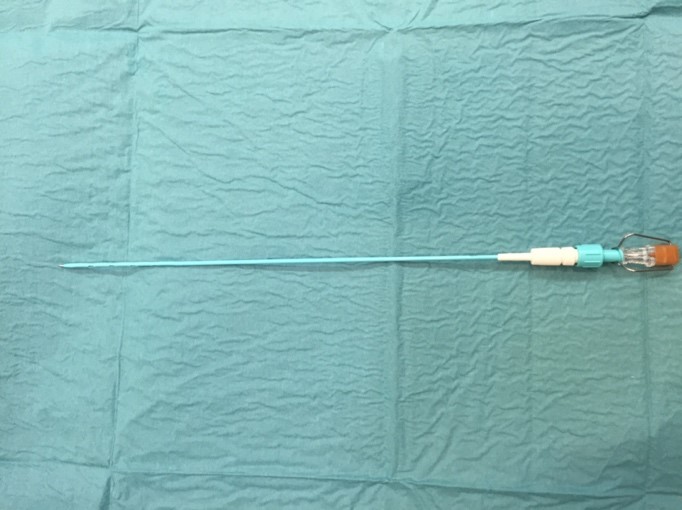
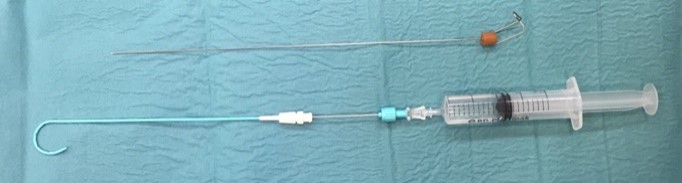
- Den solide metalnål fjernes uden at trokar eller kateter ændrer position.
- En sprøjte påsættes trokaren. Ved pneumothorax bør sprøjten indeholde saltvand, hvor man kan se bobler ved aspiration, og ved pleuraeffusion bør sprøjten være tom så pleuravæske kan aspireres. Når der ikke er en sprøjte påsat, anbefales det at holde tommelfingeren over drænets ende.
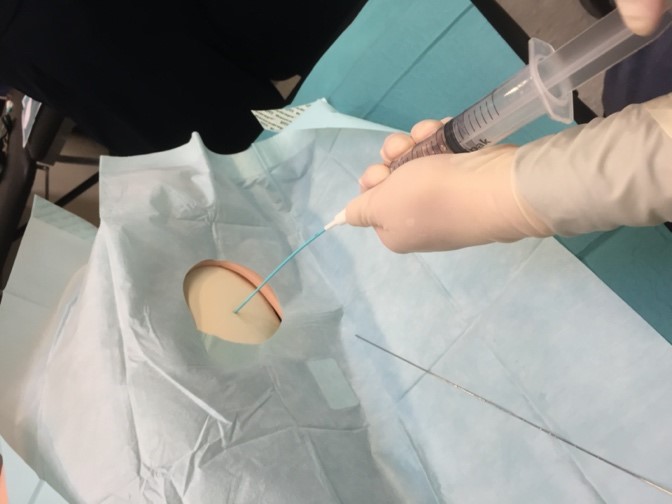
- Nu føres kateteret med den ene hånd frem over trokaren indtil der kun er 2-3 cm af kateteret synligt udenfor thorax. Hold trokaren stille med den anden hånd. Det er vigtigt at trokarens position er uændret indtil drænet er ført helt ind. Ved pneumothorax vil man typisk forsøge at føre drænet apikalt, mens man ved væske, vil føre drænet basalt.
- Forsøg ikke at genindsætte trokaren ved problemer, da dette medfører risiko for at perforere kateteret og efterlade en del af kateteret i pleura.
- Fjern trokaren.
- Fastgør trevejshane og pose med ensretterventil som sikrer, at luft og væske kun kan løbe væk fra patienten.
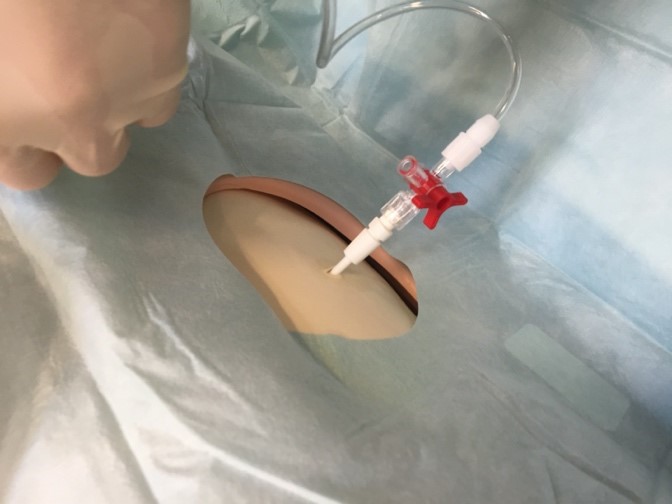
- Aspirer eventuelt luft eller væske med en sprøjte, f.eks. 50ml flere gange, både for at lindre patienten og for at sikre at drænet fungerer.

- Påfør det specialdesignede drænplaster for at holde drænet på plads.
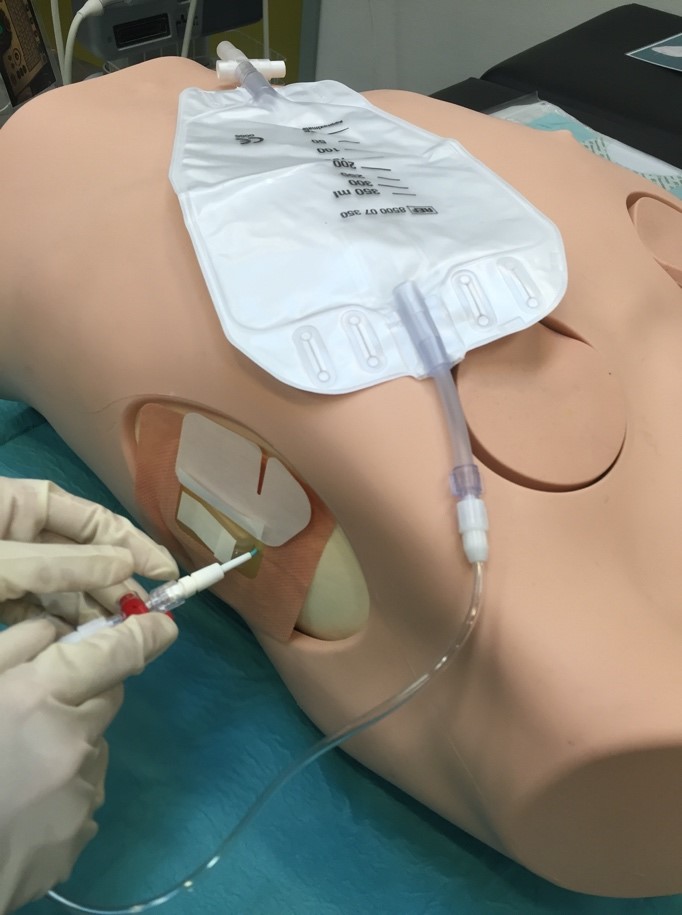
- I tilfælde hvor drænet skal blive siddende længere tid eller hvor risikoen for accidentel seponering er stor, kan man overveje at suturere drænet til huden.
- I tilfælde hvor man blot ønsker pleuracentese, men hvor der ikke er behov for at drænet bliver liggende, kan man fjerne drænet så snart, man har dræneret den ønskede mængde uden behov for fiksering af drænet.
1.9 OPLÆRING
Drænanlæggelse er en teknisk færdighed som skal trænes for at opnå mestring. Den uddannelsessøgende læge bør gøre sig fortrolig med det benyttede udstyr inden første drænanlæggelse med særligt fokus på at håndtere drænet. Såfremt det er muligt, bør drænanlæggelse trænes på fantom, før proceduren forsøges i klinikken. Der findes kurser til struktureret oplæring på bl.a. CAMES.
Indtil operatøren er kompetent i proceduren bør denne ske under supervision med fokus på tryghed og sikkerhed for både operatør og patient.
1.10 SUG
Ved pleuraeffusion, empyem og hæmothorax vil der sjældent være behov for sug og ansamlingen kan passivt dræneres til en lukket pose (”kateterpose”).
Ved pneumothorax er der et behov for, at luften kan komme væk fra pleura uanset størrelsen af luftspildet. Der er grundlæggende tre systemer. Pose eller ”boks” med Heimlichventil (som f.eks. Tru-Close™ drænet med indlejret ventil), vandlås og elektroniske sugeaggregater (Thopaz™).
Der findes systemer med Heimlichventil, hvor sug kan tilsluttes, men som udgangspunkt foregår drænagen passivt.
Tilsluttes drænet vandlås, opnås ved placering af vandlås under thoraxniveau et svagt passivt sug. Hvis indiceret, f.eks. pga. progression af subcutant emfysem eller manglende udfoldning af lungen, kan man applicere sug for at øge det negative tryk i drænhulen. Ved brug af sug på vandlås tilsluttes drænkassen suget monteret på væggen, hvormed suget binder patienten til sengen eller dennes umiddelbare nærhed, hvilket er uhensigtsmæssigt i forhold til mobilisering af patienten.
De elektroniske sugeaggregater (Thopaz™) har fordel af at være relativt lette, mobile og uafhængige af eksternt sug, hvorved mobilisering muliggøres. Sugestyrken er let at justere og ydermere aflæses størrelsen af drænage af både luft og væske kontinuerligt, sådan at man kan aflæse både øjeblikkeligt flow i drænet samt data fra de sidste 72 timer. Dette kan være hjælpsomt, når man skal vurdere, hvornår drænet kan seponeres (11).
Der er ikke konsensus om, hvilken sugestyrke der er den mest korrekte. Generelt anbefales det ved pneumothorax at begrænse suget mest muligt og kun øge sugestyrken ved progression af pneumothorax og subkutant emfysem, da data antyder, at helingen forsinkes af øget sugestyrke (14). Vi foreslår at man starter med sug på -5cm H2O.
1.11 DRÆNFJERNELSE
Der er ikke konsensus om kriterier for drænfjernelse.
Lungen tilstræbes at være udfoldet, men dette kan i nogle situationer ikke opnås (malign sygdom eller empyem).
Ved væske bør drænproduktionen være under 200 ml/døgnet (15).
Ved pneumothorax og brug af vandlås må der ikke være boblen i vandlåsen. Eventuelt kan luftspild testes ved at tilslutte en kateterpose med ventil på drænet og observere nogle timer om den fyldes med luft (obs for trykpneumothorax!).
Ved elektroniske aggregater kan flowet aflæses. Det anbefales som udgangspunkt, at der har været flow < 20ml/min i minimum 12 timer (14).
Seponering foregår ved, at eventuelle suturer løsnes, forbindingen gøres klar, og patienten instrueres i at holde vejret (enten efter en inspiration eller expiration), hvorefter drænet trækkes ud og forbindingen påsættes (16). Ved store dræn eller gabende sår sættes sutur.
1.12 KOMPLIKATIONER
Pleuradrænanlæggelse er en risikoprocedure, men alvorlige skader er dog sjældne. Komplikationsraten er større for store dræn end små dræn.
Hyppigste komplikation ved drænanlæggelse er smerter under anlæggelse og efterfølgende som følge af drænets kontakt med pleura. Omhyggelig information, velanlagt lokalanalgesi og derefter fast smertelindrende behandling reducerer smerter. Andre komplikationer er accidentel drænseponering og drændysfunktion pga tilstopning. Ved korrekt aseptisk teknik er sårinfektion og empyem sjældne.
Ved ultralydsvejledt pleuracentese er risiko for pneumothorax 4% (uden ultralyd: 9%)(17). Blødning ses hos knap 1%. Re-ekspansions-lungeødem er ekstremt sjældent (0,01%), hvis man tømmer 1,5-2,0L væske ad gangen. Hvis alt er fredeligt (patient bedres, ingen central trykken eller vedvarende hoste), så kan drænage fortsættes (18). Der er sjældent behov for at drænere mere end 3L væske. Hvis i tvivl: lad drænet blive liggende, giv peroral væske og genoptag drænage 3 timer senere. Organskade efter drænplacering i lever, milt, nyrer, hjerte er beskrevet, men er ved ultralydsvejledt procedure heldigvis sjælden (15,19).
1.13 OPFØLGNING
Afhængig af indikation. Se selvstændige vejledninger.
1.14 KREDITERING
Alle billeder tilhører CAMES.
1.15 REFERENCER
- MacDuff A, Arnold A, Harvey J. Management of spontaneous pneumothorax: British Thoracic Society pleural disease guideline 2010. Thorax. 2010;65(SUPPL. 2).
- Nielsen J, Meyer CN, Rosenlund S. Outcome and clinical characteristics in pleural empyema: A retrospective study. Scand J Infect Dis [Internet]. 2011 Jul 2 [cited 2017 Jan 10];43(6–7):430–5. Available from: http://www.tandfonline.com/doi/full/10.3109/00365548.2011.562527
- Bhatnagar R, ChB M, Maskell NA. Treatment of Complicated Pleural Effusions in 2013. Clin Chest Med [Internet]. 2013 [cited 2017 Mar 28];34:47–62. Available from: http://ac.els-cdn.com.ep.fjernadgang.kb.dk/S0272523112001220/1-s2.0-S0272523112001220-main.pdf?_tid=00f28900-138c-11e7-b33f-00000aacb35d&acdnat=1490687949_faac838cdff439718490302031c3ad5b
- Christopoulou-Aletra H, Papavramidou N. “Empyemas” of the Thoracic Cavity in the Hippocratic Corpus. Ann Thorac Surg. 2008 Mar;85(3):1132–4.
- Monaghan SF, Swan KG. Tube Thoracostomy: The Struggle to the “Standard of Care.” Ann Thorac Surg. 2008 Dec;86(6):2019–22.
- Munnell ER. Thoracic drainage. Vol. 63, Annals of Thoracic Surgery. 1997. p. 1497–502.
- HOWE BE. Evaluation of chest suction with an artificial thorax. Surg Forum [Internet]. 1951 [cited 2020 Jan 20];1–7. Available from: http://www.ncbi.nlm.nih.gov/pubmed/14931188
- Davies HE, Davies RJO, Davies CWH, BTS Pleural Disease Guideline Group. Management of pleural infection in adults: British Thoracic Society Pleural Disease Guideline 2010. Thorax [Internet]. 2010 Aug [cited 2017 Jan 10];65 Suppl 2(Suppl 2):ii41-53. Available from: http://www.ncbi.nlm.nih.gov/pubmed/20696693
- Sachdeva A, Shepherd RW, Lee HJ. Thoracentesis and Thoracic Ultrasound: State of the Art in 2013. Clin Chest Med [Internet]. 2013;34(1):1–9. Available from: http://dx.doi.org/10.1016/j.ccm.2012.11.005
- Lichtenstein D. Novel approaches to ultrasonography of the lung and pleural space: Where are we now? Vol. 13, Breathe. European Respiratory Society; 2017. p. 100–11.
- Gilbert S, McGuire AL, Maghera S, Sundaresan SR, Seely AJ, Maziak DE, et al. Randomized trial of digital versus analog pleural drainage in patients with or without a pulmonary air leak after lung resection. J Thorac Cardiovasc Surg. 2015 Nov 1;150(5):1243–51.
- Mahmood K, Wahidi MM. Straightening Out Chest Tubes. Clin Chest Med [Internet]. 2013 [cited 2020 Jan 27];34(1):63–71. Available from: https://www-clinicalkey-com.ep.fjernadgang.kb.dk/#!/content/playContent/1-s2.0-S0272523112001256?returnurl=null&referrer=null
- Clementsen PF, Lehnert P, Kandler K, Hertz P, Rasmussen KMB, Saghir Z, et al. Chest tube drainage; Treatment of Pleural Effusion (pleuracentesis) and Pneumothorax – A practical handbook.
- Holbek BL, Christensen M, Hansen HJ, Kehlet H, Petersen RH. The effects of low suction on digital drainage devices after lobectomy using video-assisted thoracoscopic surgery: a randomized controlled trial†. Eur J Cardio-Thoracic Surg [Internet]. 2019 Apr 1 [cited 2020 Jan 28];55(4):673–81. Available from: https://academic.oup.com/ejcts/article/55/4/673/5184850
- Havelock T, Teoh R, Laws D, Gleeson F. Pleural procedures and thoracic ultrasound: British Thoracic Society pleural disease guideline 2010. Thorax. 2010 Aug;65(SUPPL. 2).
- Bell RL, Ovadia P, Abdullah F, Spector S, Rabinovici R. Chest tube removal: end-inspiration or end-expiration? J Trauma. 2001 Apr;50(4):674–7.
- Gordon CE, Feller-Kopman D, Balk EM, Smetana GW. Pneumothorax Following Thoracentesis: A Systematic Review and Meta-analysis. Arch Intern Med [Internet]. 2010 Feb 22;170(4):332–9. Available from: https://doi.org/10.1001/archinternmed.2009.548
- Ault MJ, Rosen BT, Scher J, Feinglass J, Barsuk JH. Thoracentesis outcomes: a 12-year experience. Thorax. 2015 Feb;70(2):127–32.
- Cantey EP, Walter JM, Corbridge T, Barsuk JH. Complications of thoracentesis: Incidence, risk factors, and strategies for prevention. Vol. 22, Current Opinion in Pulmonary Medicine. Lippincott Williams and Wilkins; 2016. p. 378–85.