1.1. DEFINITION
Interstitielle lungesygdomme (ILS) er en heterogen gruppe af lungesygdomme, der kan opstå sekundært til miljøpåvirkning, medicin, underliggende autoimmun sygdom eller ukendte årsager (idiopatisk). ILS kan vise sig ved inflammation med efterfølgende fibrosedannelse eller alene ved fibrose, alle radiologiske forandringer, der kan identificeres på HRCT.
I takt med at flere og flere patienter får foretaget scanninger af eller involverende thorax på forskellige indikationer identificeres tilfældige radiologiske forandringer i højere grad. En del af disse forandringer ligner de forandringer som ses ved ILS, men forandringerne er ofte beskedne eller ikke associeret med symptomer eller lungefunktionsnedsættelse. Disse forandringer kaldes interstitielle lungeabnormaliteter (ILA).
ILA er en radiologisk diagnose defineret ved:
- Tilfældigt identificerede, ikke-lejringsbetingede forandringer som matglasforandringer, retikulering, lungedistortion/skrumpning, traktionsbronkiektasier, bikagetegning og non-emfysematiske cyster.
- Involvering af mindst 5% af en lungezone[1], uanset hvilken
- Forekommende hos individer, hvor man ikke mistænker ILS.
ILA subkategoriseres til:
- Non-subpleural ILA
- Subpleural non-fibrotisk ILA
- Subpleural fibrotisk ILA
1.2. FOREKOMST
ILA identificeres i stigende grad som tilfældige fund på CT Thorax eller på scanninger af thorax og abdomen og dermed også hos patienter, der ikke har respiratoriske symptomer. Prævalensen af ILA hos ældre (>60 år) er i større undersøgelser estimeret til 4-9% hos rygere og 2-7% hos ikke-rygere.
1.3. ÆTIOLOGI
ILA kan være forløber for ILS og kan således også have forskellig underliggende ætiologi som for ILS.
1.4. SYMPTOMER OG KLINISKE FUND
Per definition er ILA et tilfældigt fund og asymptomatisk, men patienter med ILA bør henvises til lungemedicinsk vurdering mhp. at afdække symptomer (dyspnø og hoste), objektive fund (clubbing og velcrokrepitation) og underliggende autoimmun sygdom (ekstrapulmonale manifestationer fra led, hud, slimhinder, muskler og øjne). Hos patienter med autoimmun sygdom men uden respiratoriske symptomer benævnes ILA per definition som præklinisk ILS.
1.5. UDREDNING
Målet med den lungemedicinske udredning er først og fremmest at identificere:
- Patienter med ILA og tegn på ILS
- Patienter med ILA med øget risiko for at udvikle lungesygdom
- Patienter med ILA uden tegn på lungesygdom
Der er sparsom evidens for håndtering af udredning af ILA. I ekspert-panel-undersøgelser er der konsensus om, at en CT-scanning med subpleural retikulering i >5% af en lungezone, traktionsbronkiektasier, bikager, centrilobulære/diffuse matglasforandringer bør følges op med en HRCT-scanning.
Der er desuden konsensus om, at udredningen af patienter med ILA bør indeholde udvidet lungefunktionsundersøgelse, uafhængig af symptomer, idet restriktivt nedsat LFU vil understøtte en præklinisk ILS, hvis andre årsager udelukkes.
Hos asymptomatiske patienter med bikagetegning eller traktionsbronkiektasier på HRCT anbefales henvisning til ILS center.
Patienter med ILA og symptomer på ILS eller tegn på systemisk sygdom skal udredes som ILS patienter efter samme tilgang som skitseret i DLS retningslinjen for ”interstitielle lungesygdomme” (se venligst denne) og består i korte træk af specifik anamnese, udvidet lungefunktionsundersøgelse, 6 min. gangtest, blodprøver og HRCT af thorax samt evt. ved behov invasiv diagnostik. med lungebiopsi og BAL.
1.6. HÅNDTERING OG PROGRESSION
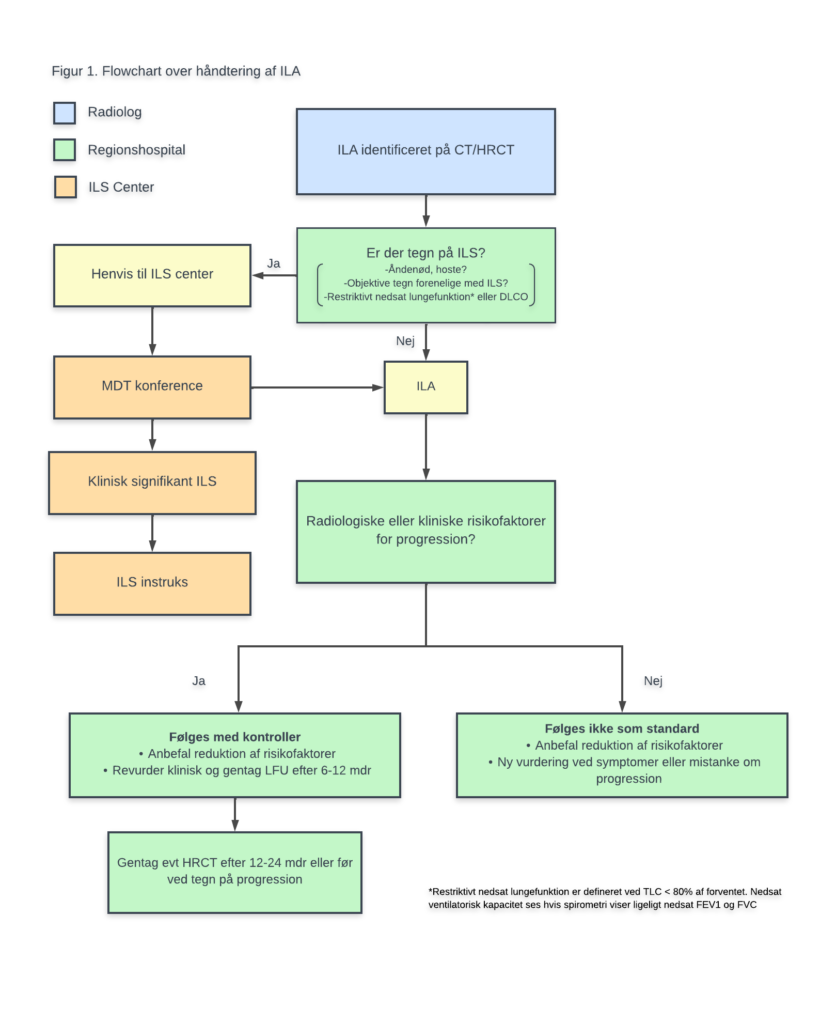
Figur 1 viser et flowchart over håndtering af ILA.
ILA kan være associeret med respiratoriske symptomer, nedsat lungefunktion, hyppigere indlæggelser, risiko for progression og øget mortalitet. Opfølgning og kontrol af patienter med ILA baserer sig på symptomer og risikofaktorer for progression
Følgende risikofaktorer er associeret med progression af ILA:
Kliniske risikofaktorer:
- Rygning
- Anden relevant inhalations-eksponering
- Medicin (kemoterapi, immunterapi)
- Stråleterapi
- Tidligere operation i thorax
- Nedsat lungefunktion
Radiologiske risikofaktorer:
- Non-fibrotiske ILA med basal og perifer prædominans
- Fibrotisk ILA med basal og perifer prædominans men uden bikager (ILA med probable UIP mønster)
- Fibrotisk ILA med basal og perifer prædominans og bikager (ILA med UIP mønster)
Patienter med ovennævnte kliniske og radiologiske risikofaktorer bør kontrolleres og kontrolscannes ved mistanke om progression. Disse patienter kan følges regionalt på lungemedicinske afdelinger, men ved progression og/eller symptomudvikling bør patienterne henvises til et ILS center. Patienter med UIP mønster har større risiko for progression og bør altid henvises til vurdering ved ILS center.
Der er ikke enighed om, hvordan og hvor længe ILA patienter skal følges op, men ekspertpaneler anbefaler, at opfølgning inkluderer udvidet lungefunktionsundersøgelse hver 6.-12. mdr. i 2-5 år.
Patienter uden risikofaktorer behøver ikke formaliseret kontrol, men bør informeres om at henvende sig, såfremt de får symptomer på nedsat lungefunktion.
1.7. PROGNOSE
ILA er associeret med højere risiko for progression og kan være en forløber for idiopatisk pulmonal fibrose (IPF) eller andre fibrotiske ILS. Den estimerede risiko for progression er 20% og 40% i løbet af hhv. 2 og 5 år. ILA generelt er associeret til øget all-cause mortalitet.
Patienter med ILA og svære traktionsbronkiektasier og/eller bikager har en overlevelse på 5,4 år (sv.t. IPF patienter) sammenlignet med 12,9 år for patienter uden ILA. Dødsårsagen i ILA gruppen var dog hyppigere kardielt end respiratorisk.
ILA er desuden associeret med øget risiko for lungekræft og ekstrapulmonal malignitet. Hos patienter med lungekræft, der får foretaget kurativt intenderet operation, har tilstedeværelsen af ILA vist at øge risikoen for komplikationer og nedsætte overlevelsen.
1.8. REFERENCER
- Hatabu H, Hunninghake GM, Richeldi L, Brown KK, Wells AU, Remy-Jardin M et al. Interstitial lung abnormalities detected incidentally on CT: a Position Paper from the Fleischner Society. Lancet Respir Med. 2020;8(7):726-737.
- Hunninghake GM, Goldin JG, Kadoch MA, Kropski JA, Rosas IO, Wells AU et al. Detection and Early Referral of Patients With Interstitial Lung Abnormalities: An Expert Survey Initiative. Chest. 2022;161(2):470-482
- Hida T, Nishino M, Hino T, Lu J, Putman RK, Gudmundsson EF, et al. Traction Bronchiectsis / Bronchiolectasis is Associated with Interstitial Lung Abnormality Mortality. Eur J Radiol. 2020;129:109073
- Im Y, Chung MP, Lee KS, Han J, Chung MJ, Kim HK et al. Impact of interstitial lung abnormalities on postoperative pulmonary complications and survival of lung cancer. Thorax. 2022 Jun 10:thoraxjnl-2021-218055.
- Nils Hoyer, Mathilde M.W. Wille, Laura H. Thomsen, Torgny Wilcke, Asger Dirksen, et al. Interstitial Lung Abnormalities are Associated with Increased Mortality in Smokers. Respiratory Medicine 2018; 136:77-82.
- Nils Hoyer, Laura H. Thomsen, Mathilde M.W. Wille, Torgny Wilcke, Asger Dirksen, et al. Increased morbidity in people with Interstitial Lung Abnormalities. BMC Pulm Med. 2020 Mar 19;20(1):67.
[1] Lungezone: Defineret ved Hatabu et al (1): øvre- mellem- og under-zone er afgrænset ved inferiore aorta og hø. V. pulmonalis.