HENT DEN KORTE VERSION SOM PDF HER
1. INDLEDNING
Astma er en af de store folkesygdomme. Det skønnes, at ca. 10% af den danske voksne befolkning lider af astma1, de fleste har mild til moderat astma. Denne vejledning er en struktureret gennemgang af behandlingstiltag for unge og voksne patienter med netop mild til moderat astma, defineret som patienter, der kan opnå god sygdomskontrol på GINA step 1-3 og dele af step 4.
Hovedpunkterne er: Valg af den initiale behandling, monitorering af behandlingseffekt samt justering af behandling.
De overordnede behandlingsmål: At opnå god symptom- og sygdomskontrol samt forebygge eksacerbationer, permanent nedsat lungefunktion og død (se prognoseafsnittet).
Vejledningen er baseret på anbefalingerne fra GINA 2019 og 2020, men tolket ind i en dansk kontekst.
Før opstart af astmabehandling skal patienten have gennemgået en systematisk udredning jf. DLS’ vejledning: https://lungemedicin.dk/astma-diagnostik/
Vejledning til behandlingen af svær astma findes i særskilt DLS’ vejledning: https://lungemedicin.dk/astma-svaer-udredning-og-behandling-af-patienter-med-mulig-svaer-astma/
Anvendte forkortelser:
ICS: Inhalationssteroid
LABA: Langtidsvirkende β2-agonister
LAMA: Langtidsvirkende muskarin antagonist (antikolinergikum)
LTRA: Leukotrien receptor antagonist
SABA: Korttidsvirkende β2-agonister
Pn.: pro necessitate/efter behov
IT: Immunterapi
AIT: Allergen immunterapi
SCIT: Subkutan immunterapi
SLIT: Sublingual immunterapi
Adherence: Begreb der beskriver med hvilke grad patienten følger behandlings plan/tiltag
2. VALG AF INITIALE BEHANDLING
Evidensen for at daglig ICS-behandling forebygger eksacerbationer og giver god symptomkontrol er meget omfattende, derfor er fast ICS et særdeles godt behandlingsvalg. Adherence til fast ICS-behandling er dog mangelfuld hos en betydelig andel af astmapatienterne. En del bruger derfor alene SABA som behandling for deres astma. Over de sidste par år er der kommet tiltagende evidens for, at SABA som monoterapi medfører øget risiko for astma eksacerbationer. Derfor anbefales SABA som monoterapi ikke længere, og det gælder ikke mindst patienter med behov for step 1 behandling, sv.t. patienter med sjældne symptomer. GINA 2019 og 2020 anbefaler lavdosis ICS/formoterol ved behov i stedet for SABA monoterapi.
Noget nyt i behandling af mild til moderat astma er netop brugen af pn. lav-dosis ICS/formoterol som patienten skal tage ved forekomst af astmasymptomer. I patientgruppe med mild og moderat astma er der evidens for at pn. ICS/formoterol beskytter lige så godt mod eksacerbationer som fast lav-dosis ICS og beskytter bedre end monoterapi med SABA.
ICS/formoterol taget ved behov kan derfor være et attraktivt behandlingsvalg til patienter med sjældne symptomer eller til patienter der ikke kan motiveres til fast inhalationsbehandling. Har patienten ikke symptomkontrol ved alene ICS/formoterol ved behov må patienten igen forsøges motiveres til brug af fast ICS-behandling enten som fast ICS eller ICS/LABA.
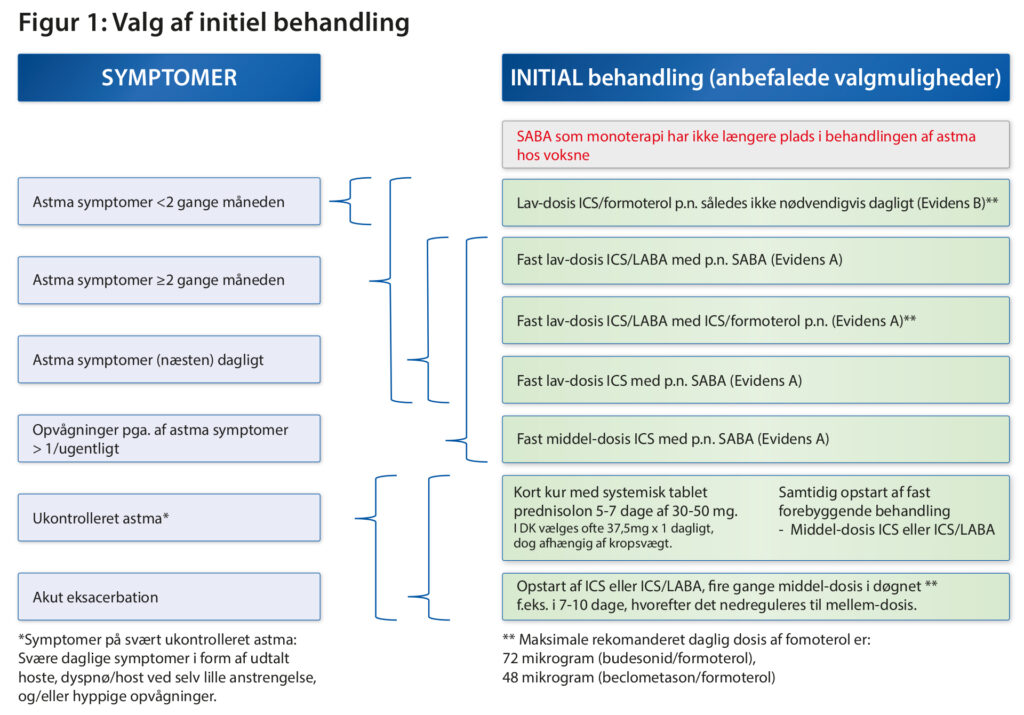
Figur 1 giver en skematisk vejledning i valg af behandling til den ny-diagnosticerede astma patient og til patienter med behov for at genoptage astmabehandling.
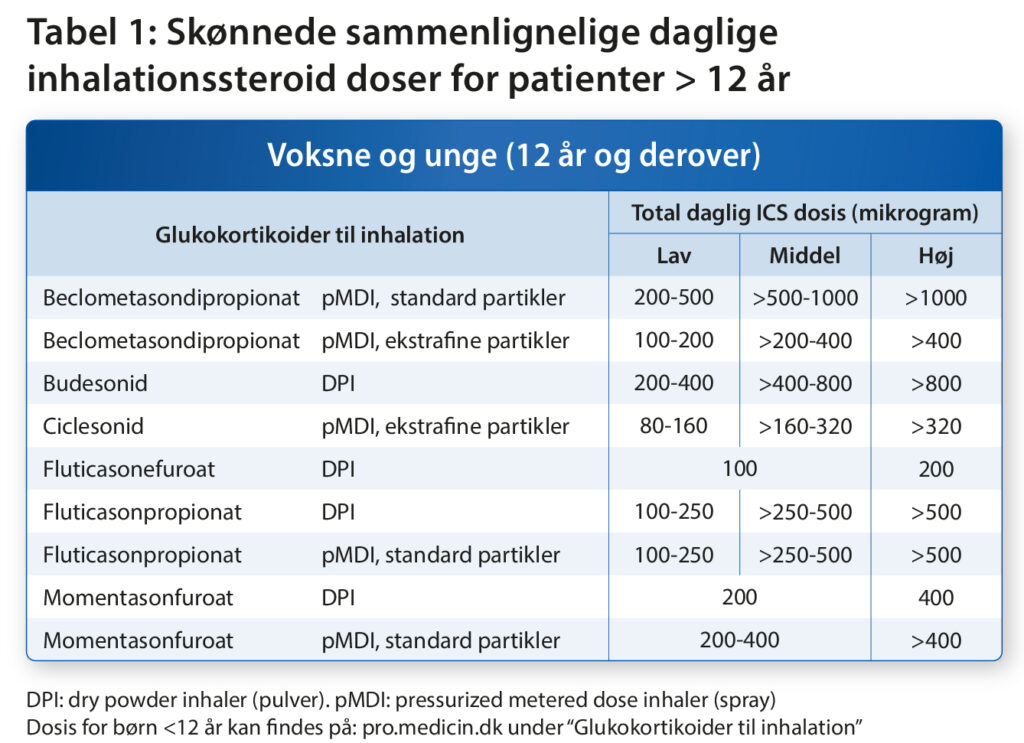
Oversigt over sammenlignelige doser af forskellig inhalationsmedicin, lav-, mellem- og høj-dosis ICS findes i tabel 1.
De fleste patienter, der henvender sig til læge med respiratoriske klager som følge at ubehandlet astma har symptomer flere gange månedligt eller næsten dagligt. Derfor vil opstart af fast ICS eller fast ICS/formoterol være relevant for de fleste patienter. Hvis der ud fra forventning om god adherence til ICS-behandling hos en patient, bedømt ud fra samtale og tidligere erfaring, vil SABA være et fint valg som pn. medicin. Vurderes patienten i risiko for dårlig adherence med fast ICS-behandling, vil ICS/formoterol som behovsmedicin være det gode valg.
Det er specifikt kombinationen ICS/formoterol, der anbefales som behovsmedicin, da det er lav-dosis ICS/formoterol der er undersøgt i randomiserede kliniske studier. Derudover har formoterol en hurtig indsættende virkning (ca. 5-15 min).
Understående oversigt over valg af initiale behandling (figur 1) indeholder primær vejledning baseret på patientens symptomer. Det er dog vigtigt at holde sig følgende for øje i forhold til astmabehandling, også ved behandlingsopstart.
- Har patienten øget risiko for fremtidige eksacerbationer (rygning, inhalations-allergi med snarlig sæson, lav FEV1, højt blod-eosinofiltal, høj FeNO, og/eller højt SABA forbrug)*(side 4)
- Er patienten i risiko for at underrapportere symptomerne og derved underbehandling (tilvænnet til astmasymptomerne grundet astma siden barndom, har nedreguleret aktivitetsniveau)
- Få, men sværere symptomer (anamnese med eksacerbationer f.eks. i forbindelse med virale luftvejs-infektioner)
I de tilfælde skal der overvejes valg af højere behandlingsniveau end den behandling, der kun er dikteret af symptomhyppighed.
En stor procentdel af astmapatienter har samtidig rhinitis, allergisk, non-allergisk, sæsonbetinget eller kronisk. Hos disse patienter skal det vurderes om nasal steroid skal opstartes som en del af den initiale behandling.
*Parametrene skal vurderes i en helhed og ift. den enkelte patient. De angivne grænser er derfor kun vejledende:
Lav FEV1: fald på >200ml i forhold til tidligere eller FEV1 under 80% af forventet
Blod eosinofiltal: >0,15-0,30 mia/L, men vægtes mere ved værdier >0,50 (se afsnit om eosinofile)
Højt SABA forbrug: over 2 ugentligt, men vægtes mere ved f.eks. 2 dagligt. Ved brug af >200 doser månedligt har patienten en øget risiko for astma-relateret død2.
3. MÅL MED ASTMA BEHANDLING OG BEHANDLINGSMONITORERING
Målene for opfølgning på astmabehandling (behandlingskontrol):
- Øge patientens sygdomsforståelse og adherence
- Opnå symptomkontrol (også under fysisk aktivitet)
- Nedsætte risikoen for eksacerbationer
- Nedsætte risikoen for astma-relateret indlæggelser
- Nedsætte risikoen for ikke-reversibel luftvejsobstruktion
- Nedsætte risikoen for astma-relateret død
Patientinddragelse i valg af behandling har vist at have stor indflydelse på om behandlingsmålene nås, og er derfor central i astmabehandling.
4. OPFØLGNING
Alle patienter med astma, uafhængig af sværhedsgraden, skal tilbydes opfølgende besøg hos egen læge, praktiserende speciallæge eller lungemedicinske ambulatorier. Hyppigheden afhænger at sværhedsgrad af astma og graden af sygdomskontrol. Alle astmapatienter skal som minimum tilbydes årlig opfølgning. Ny-diagnosticerede patienter, der sættes i behandling, skal kontrolleres gerne 3 måneder, men senest 6 måneder efter behandlingsopstart for at sikre effekt og validere diagnosen.
Det centrale ved opfølgningen af astmapatienter kan deles op i tre overordnede punkter jf. tabel 2.

Det er vigtigt at være opmærksom på at en stor andel af astmapatienter har en allergisk astma. Understående vejledning omkring opfølgning og justering af behandlingen er gældende også for fænotypen allergisk astma. Dog anbefales der særlige tiltag for allergisk astma, de beskrives samlet under afsnittet ”Patienter med allergisk astma”.
4.1. VURDERE EFFEKTEN AF TILTAG/BEHANDLING
4.1.1. Symptomer:
Et vigtigt element i vurderingen af astma-kontrol er hyppighed og sværhedsgrad af symptomer (tabel 3).

4.1.2. Vurdering af risiko for eksacerbationer:
Især manglende symptomkontrol og lav FEV1 øger risikoen for eksacerbationer. Andre faktorer har også betydning.
Faktorer, der øger risikoen for eksacerbationer:
- Manglende symptom kontrol
- Lav/fald i FEV1
- Eksponering for tobaksrøg
- Allergen eksponering
- Allergisk rhinitis
- Kronisk rhinosinuitis (CRS)
- Højt forbrug af SABA
- Svær eksacerbation i de sidste 12 måneder
- Forhøjet FeNO
- Forhøjet blod eosinofiltal
- Overvægt
Vurderes risikoen for fremtidige eksacerbationer stor, kan man overveje opjustering af astmabehandling trods få symptomer.
4.1.3. Lungefunktion:
Selvom der ikke nødvendigvis er en stærk korrelation mellem astma patienters symptomhyppighed og patientens lungefunktion, er et fald i FEV1 en kendt stærk prædiktor for fremtidig eksacerbation. En patient med tydeligt fald i FEV1 er derfor i øget risiko for eksacerbationer og som følge her af i manglende astma kontrol. FEV1 skal sammenlignes med sidst målte FEV1 og med patientens ”bedste personlige FEV1”.
Lungefunktionsmåling er vigtig i forbindelse med løbende evaluering af astma, diagnose og risiko. FEV1 kan naturligt variere op til 12-15% og er derfor ikke velegnet som selvstændigt mål for graden af astmakontrol. Et fald i FEV1 i den størrelsesorden uden andre tegn på manglende sygdomskontrol, skal derfor tolkes med forsigtighed.
4.1.4. Peakflow monitorering:
Enkelte astma patienter kan have gavn af at monitorere deres peakflow med henblik på vurdering af sygdomskontrol. Det findes særligt anvendelig i de tilfælde, hvor andre årsager til dyspnø vanskeliggør en vurdering af astmasymptomerne. Det kan f.eks. være angst, hjertesygdom og patienter med dårlig kropsforståelse/opfattelse.
4.1.5. Måling af FeNO og blod eosinofile:
Hvis tilgængelig kan FeNO måling være et fint supplement til kontrol af den eosinofile astma, såvel non-allergisk som allergisk. Ved værdier under 25 ppb er sandsynligheden for eosinofil luftvejsinflammation lille, hvorimod et niveau på over 50 ppb indikerer høj sandsynlighed for eosinofil inflammation og prædikterer et godt respons på inhalationssteroid. Ændring på 8 ppb er en sikker ændring. Faldende værdier tyder på forbedring, mens en stigning tyder på en forværring. Også her er kendskab til patientens personligt bedste værdi (= laveste) af stor værdi i monitoreringen af sygdommen.
Måling af blod eosinofile anvendes i monitoreringen af svær og/eller vanskeligt behandlelig astma på lungemedicinske ambulatorier. Vedvarende blod-eosinofile > 0.3 mia/L, uden anden kendt årsag, tyder på eosinofil luftvejsinflammation.
Bruges FeNO og blod eosinofilocytter i astmakontrol bør man tage med i overvejelserne, hvilke andre tilstande, der påvirker det målte niveau. Tilstande som rhinitis, nasal eosinofili, infektion (almindeligt forekommende og mere eksotiske som f.eks. parasit infektion), rygning og mange andre tilstande kan påvirke de målte værdier (oversigt kan findes på f.eks. uptodate.com).
Både FeNO og blod eosinofile kan bruges som surrogat mål for eosinofil luftvejsinflammation og kan derfor bruges til klassificering af astmatypen eosinofil astma. Der ses nemlig er sammenhæng mellem FeNO og blod eosinofilocytter, dog ikke lineær, samt en sammenhæng mellem forekomsten af eosinofile celler i blod og induceret sputum. Dog udelukker lav FeNO og lave blod-eosinofile ikke eosinofil astma. BAL og induceret sputum er en mere sikker metode til at be- eller afkræfte eosinofil luftvejsinflammation.
Antallet af neutrofile granulocytter i perifert blod kan ikke anvendes til at vurdere eventuel neutrofil luftvejsinflammation.
4.1.6.Bivirkninger af ICS:
Valg af behandling skal ske under hensyntagen til både forventet effekt og risiko for bivirkninger. Fast langtidsbehandling med højdosis ICS giver sjældent øget behandlingskontrol3, men øger risikoen for både systemiske og lokale bivirkninger, som tendens til blå mærker, øget risiko for udvikling af diabetes, fald i knoglemineraltætheden, oral candidiasis, hæshed og irritationshoste. Af den grund anbefales højdosis ICS som hovedregel kun i få måneder. Ved relevant dosis, men samtidig bivirkninger, er der indikation for at skifte behandling til et andet device eller steroid.
4.2. VURDERE ÅRSAG TIL UTILSTRÆKKELIG BEHANDLINGSEFFEKT
4.2.1. Mangelfuld adherence:
Manglende adherence er en hyppig og problematisk årsag til utilstrækkelig effekt af behandlingen. Adherence skal derfor vurderes ved hver astma opfølgning. Vurdering på baggrund af receptindløsninger ved opslag i FMK anbefales. En stigning i FeNO kan fint være forårsaget alene af manglende adherence til ICS-behandlingen.
4.2.2. Mangelfuld inhalationsteknik:
Suboptimal inhalationsteknik er ligeledes en hyppig årsag til utilstrækkelig effekt af behandlingen4, men oftest let korrigerbar. Patienters inhalationsteknik bør kontrolleres ved introduktion af nyt device og derefter regelmæssigt. Som vejledning til kontrol af patientens inhalationsteknik kan en checkliste anvendes (se checkliste i DLS’ vejledningen ”Udredning og behandling af patienter med mulig svær astma”). Alternativt findes der brugbare instruktionsvideoer på pro.medicin.dk og min.medicin.dk under de enkelte præparater.
4.2.3. Rygning:
Eksponering for både aktiv og passiv rygning er forbundet med betydelig øget risiko for manglende astmakontrol. Aktiv tobaksrygning, og i mindre grad passiv rygning, kræver behandling med øget ICS dosis for at opnå sygdomskontrol og giver med tiden desuden en betydelig øget risiko for udvikling af ikke-reversibel luftvejsobstruktion.
4.2.4. Allergen eksponering:
Se afsnit om patienter med allergisk astma
4.2.5. ko-morbiditet:
Især vurdering af samtidig rhinitis og dyspepsi er anbefalet. Begge tilstande kan i sig selv give hoste, men kan hos astmapatienter bidrage til forværring af deres astma.
Oversigt over de fleste ko-morbiditeter ved astma findes i DLS’ vejledningen ”Udredning og behandling af patienter med mulig svær astma” Tabel 4.
Fedme er ligeledes en ko-morbiditet der har indflydelse på både selve inflammationen i luftvejene, men også på symptombyrden (Se afsnittet om non-farmakologisk behandling i denne instruks).
4.2.6. Revurdering af astma-diagnose:
Efter en grundig vurdering af adherence, inhalationsteknik og relevant håndtering af andre faktorer, der kan forårsage utilstrækkelig effekt, skal manglende effekt af ICS/forebyggende astma-behandling medføre en revurdering af baggrunden for astmadiagnosen. Foreligger der en positiv astma-test? Var primær klage oplagt forenelig med astma eller drejede det sig om mono-
symptomatisk hoste eller åndenød. Manglende/tvivlsom effekt af ICS skal føre til evaluering af astmadiagnosen.
4.3. BEHANDLINGSTILTAG
Behandlingstiltag skal målrettes de faktorer, der for den enkelte patient bidrager til utilstrækkelig effekt af behandlingen. Først derefter vurderes det, om der er behov for justering af den medicinske behandling.
Der har tidligere været en tendens til hurtigt at øge ICS dosis. Det er dog vigtigst at have fokus på øvrige faktorer til behandlingssvigt, da hovedparten af astma patienter ikke vil opnå øget effekt af mellem til højdosis ICS, men derimod øget risiko for bivirkninger4,5.
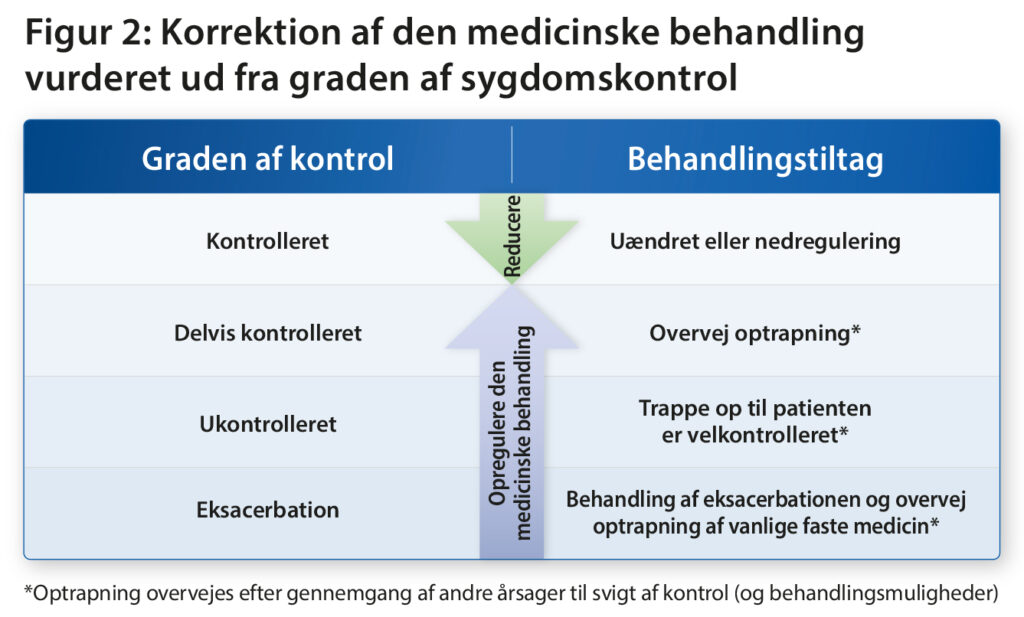
4.3.1. Medicin justering:
Den medicinske op og nedjustering skal se på baggrund af graden af astmakontrol (Figur 2). Medicin op og nedjustering gøres som udgangspunkt trinvis efter GINAs behandlingsvejledning (figur 3).
5. OPTRAPNING AF DEN MEDICINSKE BEHANDLING
Medicin opjustering gøres som udgangspunkt trinvis efter GINAs behandlingsvejledning (figur 3). Vurderes det nødvendigt at øge den medicinske behandling, vælges der som udgangspunkt at trappe et behandlingstrin op ad gangen.
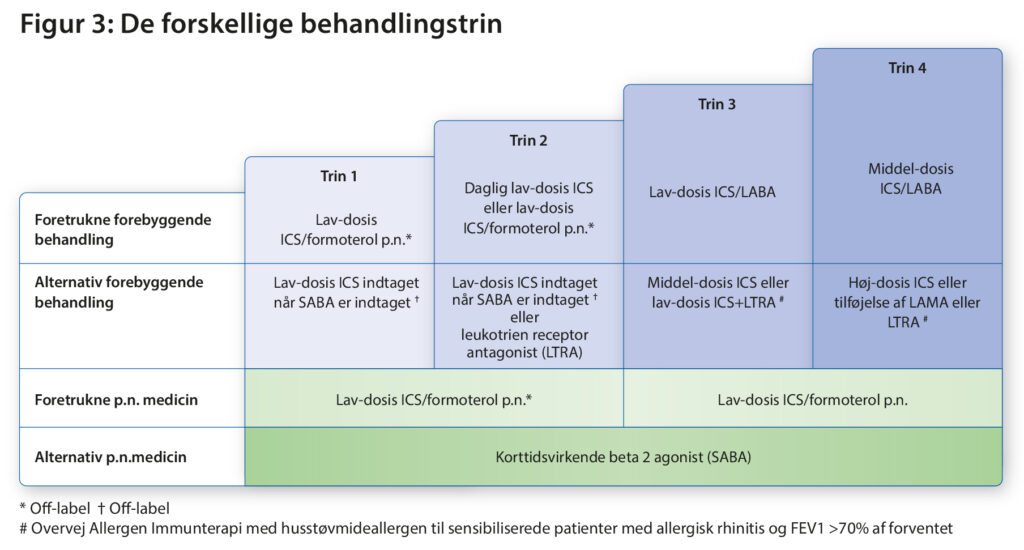
5.1. TRINVIS OPTRAPNING
5.1.1. Trin 2:
Lav-dosis ICS taget fast er vist effektivt ved talrige randomiseret studier, hvorfor det er den anbefalede medicinske behandling hos langt de fleste patienter. ICS/formoterol tages efter behov er en sikkert alternativ især til patienter med dårlig adherence.
Patientuddannelse og patientinddragelse mhp. at øge patientens sygdomsforståelse og adherence skal ikke tænkes at være mindre vigtigt ved valget af ICS/formoterol behandling.
5.1.2. Trin 3:
Giver valgmulighed mellem tre forskellige behandlingsformer:
- Lav-dosis ICS/LABA
- Mellem-dosis ICS
- Lav-dosis ICS+LTRA.
I et Cochrane review findes tillæg af LABA til lav-dosis ICS moderat mere effektivt end ved tillæg af LTRA6.*
Som der nævnes under ko-morbiliteter og under AIT-afsnittet er det vigtigt, at astma patienter er velbehandlede for en eventuel samtidig allergisk rhinitis, her nævnes også at AIT er en relevant behandling for nogle patienter med allergisk astma. Et stort klinisk randomiseret studie har vis at SLIT for husstøvmider medfører en reduktion i behovet for ICS hos astma patienter med husstøvmideallergi og allergisk rhinitis7. Af den grund bør AIT behandling overvejes hos astma patienter allerede ved manglende kontrol på trin 3, hvis vurderingen er, at allergien er et væsentligt element i sygdomsbilledet
5.1.3. Trin 4
Jævnfør Figur 3 vil opjustering af astmabehandlingen til trin 4 give følgende behandlingsvalg:
- Opjustere til mellem-dosis ICS/LABA
- Opjustering til høj-dosis ICS
- Tillæg af LTRA (til lav-dosis ICS/LABA eller mellem-dosis ICS)
- Tillæg af LAMA (til lav-dosis ICS/LABA eller mellem-dosis ICS)
Er patienten ikke velbehandlet på trin 4 trods fokus på faktorer nævnt i tabel 2 er patienten at betragte som ”difficult to treat” alternativt har de svær astma.
Vejledning om håndtering af den patientgruppe ligger i instruksen: https://lungemedicin.dk/astma-svaer-udredning-og-behandling-af-patienter-med-mulig-svaer-astma/
Justering af ICS hos patienter med allergisk astma:
Se afsnittet om patienter med allergisk astma.
5.2. ANDEN MEDICINSK BEHANDLING
5.2.1 LTRA:
Enkelte patienter oplever god effekt af leukotrien receptor antagonist (LTRA) behandling, hvorfor det anbefales at afprøve LTRA (10 mg dagligt til voksne, 5mg til børn) især hos patienter med allergisk rhinitis og astma, anstrengelsesudløst astma, samt til astma patienter med NSAID/ASA induceret forværring af astmasymptomer. Ved manglende effekt efter op til tre måneders behandling, kan LTRA seponeres. LTRA kan anvendes i step 2-5. Monoterapi med LTRA til voksne med astma (Gina step 2) anbefales som hovedregel ikke i Danmark, da LTRA er mindre effektiv end ICS på forebyggelse af eksacerbationer8.
Som behandler skal man være opmærksom på at LTRA kan forårsage neuropsykiatriske hændelser, i form af onde drømme, ekstremt sjælden i form af f.eks. hallucinationer eller desorientering (se evt. produktbeskrivelsen).
5.2.2. LAMA:
Et stigende antal randomiserede kliniske studier har undersøgt effekten af LAMA behandling til astma patienter som tillæg til ICS og ICS/LABA. LAMA som add-on terapi til ICS og ICS/LABA har vist at kunne reducere eksacerbationer og dermed øge astma kontrol, hvilke kan medføre mindre behov for systemisk steroid og biologisk behandling.
5.2.3. Azithromycin:
Er en off-label behandling til patienter med moderat/svær eosinofil og non-eosinofil astma og anbefales ikke som behandling for mild til moderat astma. Mere om azithromycin-behandling kan findes i DLSs vejledning om svær astma.
5.2.4. Allergen immunterapi (IT):
Se afsnittet om patienter med allergisk astma.
5.2.5. Influenza-vaccination:
I et stort review af placebo-kontrollerede randomiserede studier har influenzavaccination ikke vist at kunne reducere astma eksacerbationer10. Senere review har dog vist en tendens til positiv effekt11. Et væsentligst fund ved dette review er, at der ikke ses øget risiko for eksacerbationer efter influenzavaccination. Findes der af andre årsager indikation for influenzavaccination af patient med mild til moderat astma, er astmadiagnosen ikke en kontraindikation. Patienter med svær astma kan ved individuel vurdering tilbydes gratis influenzavaccination jf. SSI’s retningslinjer om behandling af kroniske lungesygehttps://www.ssi.dk/vaccinationer/influenzavaccination.
6. NON-FARMAKOLOGISK BEHANDLING (EKSTRA-PULMONALE BEHANDLINGSSTRATEGIER)
6.1. RYGESTOP
Andelen af astmapatienter, der starter med at ryge svarer desværre til baggrundsbefolkningen. Rygning øger inflammationen i luftvejene. Derfor er rygestop helt central for at opnå velkontrolleret astma, men også for at reducere risikoen for eksacerbationer og forebygge udviklingen af persisterende luftvejsobstruktion. Af samme årsager skal patienter med astma forsøge at undgå passiv tobakseksposition.
6.2. VÆGTREDUKTION
Det er vist, at 5-10% vægttab hos overvægtige kan forbedre astma kontrol12,13. Overvægt og fedme bør være et vigtigt target i behandling af astma, da både inflammationen i luftvejene, systemisk inflammation og symptomerne forværres ved fedme.
6.3. FYSISK TRÆNING
Aerob træning har positiv effekt på astmakontrol og lungefunktionen hos voksne, men det tyder ikke på, at træning ændrer graden af inflammation i luftvejene14.
6.4. NEDSÆT ALLERGEN EKSPOSITION I HJEMMET
Se afsnittet om patienter med allergisk astma.
7. NEDTRAPNING AF INHALATIONSMEDICIN
Før nedjustering af den medicinske behandling skal patienten have været velkontrolleret i længere tid, minimum 3 måneder, men ofte gerne længere afhængig af sygdomshistorik, bl.a. hvor svært det har været at opnå god sygdomskontrol.
Det er vigtigt at følgende ting er opfyldt før nedregulering den medicinske behandling overvejes:
- Ingen eksacerbationer de sidste 12 måneder
- Astma symptomer under 2 gange månedlig
- Ikke tæt på sæson, der hyppigt giver patienten forværringer (vinterhalvår, pollensæson)
- Ingen pågående infektioner
Der skal gennemføres opfølgning på astmabehandlingen efter enhver nedregulering af den medicinske behandling. Opfølgningen skal indeholde de vanlige elementer som beskrevet i tabel 2. Patienten skal grundigt instrueres i at monitorere egne symptomer samt at søge læge ved tegn på svigt af astma kontrol.
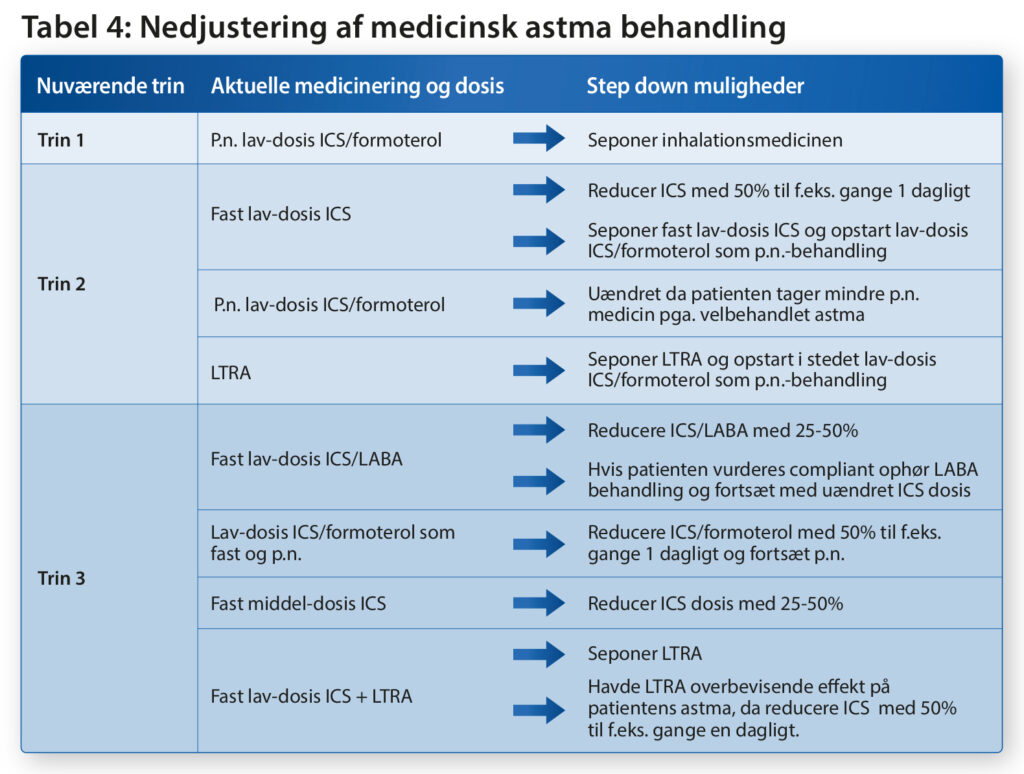
En større metaanalyse har fundet at nedregulering af ICS med 25-50% med 3 måneders opfølgning er sikkert for patienterne15. Forslag til nedregulering findes i tabel 5.
Det er vigtigt her at påpege, at SABA som monoterapi ikke anbefales, heller ikke som sidste trin i nedtrapning af astma-behandlingen.
8. BEHANDLING AF KO-MORBIDITET
En ubehandlet rhinitis, kronisk rhinosinusitis med eller uden nasale polypper kan forværre inflammationen i de nedre luftveje og derved være en af årsagerne til manglende kontrol af astma. Behandling af disse tilstande er derfor vigtig.
Gastroesophageal refluks kan udover at forværre astma i sig selv give irritationshoste og forårsage unødvendig opjustering at astmamedicin.
I DLS’ vejledning https://lungemedicin.dk/astma-svaer-udredning-og-behandling-af-patienter-med-mulig-svaer-astma/ findes der i tabel 4 en fin oversigt over behandling af ko-morbiditeter.
8.1. ACETYLSALICYLSYRE/NSAID-FORVÆRRING AF ASTMA
Hos enkelte patienter kan ASA eller NSAID præparater forværre deres astma og/eller rhinitis. Er der historik for betydende forværring må præparaterne undgås. Tilstanden kaldes Aspirin-exacerbated respiratory disease (AERD) eller NSAID-exacerbated respiratory disease (NERD).
9. PATIENTER MED ALLERGISK ASTMA
9.1. ALLERGEN EKSPONERING
Luftbårne inhalationsallergener kan medføre forværring af den allergiske astma, enten i form af sæsonbetinget øget inflammatorisk proces med øget risiko for forværringer (pollen) eller helårs provokation af th2 inflammationen (husstøvmider). Patienter med allergi for pollen kan have brug for øget medicinering forud for eller i sæsonen. Ko-morbiditet i form af allergisk rhinitis er hyppigt forekommende (60%) og fast nasal steroid spray er ofte en vigtig behandling både for at opnå kontrol med den nasale inflammation og for astmakontrollen.
Allergi for husdyr/kæledyr, der forekommer i hjemmet, vil kræve øget behandling med ICS for at opnå kontrol med sygdommen. Anskaffelse af kæledyr i familier med allergi anbefales generelt ikke.
9.2. NEDSÆT ALLERGEN EKSPOSITION I HJEMMET
Hos patienter med allergisk astma kan det have effekt at nedsætte allergeneksponeringen i hjemmet, men evidensen er ikke omfattende.
For patienter med allergi for husstøvmider anbefales simple tiltag for at nedsætte allergeneksponeringen. Grundig udluftning, afdampning af seng inden den redes og hyppig 60 graders vask af sengelinned og -tøj anbefales hos alle med husstøvmideallergi (Sengetøj hver 14. dag, dyner og hovedpuder 4 x årligt). Tæpper og gardiner, især i soverum, skal om muligt fjernes. Specielt fokus bør overvejes på sommerhuse og campingvogne, hvor forekomsten af husstøvmider kan være højt, hvis sengetøjet f.eks. har været gemt væk siden sidste år.
Hos patienter med pelsdyrsallergi vil fjernelse af det pågældende husdyr fra hjemmet nedsætte luftvejsinflammationen16. Derfor skal patienten guides i retning af, at det pågældende dyr ikke er i hjemmet. Hvis dyret tidligere har boet i hjemmet og fjernes, skal familien forberedes på, at det kan tage måneder før allergenniveauet i hjemmet reduceres.
9.3. JUSTERING AF ICS HOS PATIENTER MED ALLERGISK ASTMA
Hos patienter, der udelukkende oplever symptomer på astma under pollensæsonen, kan inhalationsbehandling for astma startes minimum 1 måned før sæsonen begynder. Det er vigtigt at skelne mellem astma forværret i pollensæsonen og astma alene i sæsonen. Grundig anamnese ift. mulig persisterende astmasymptomer/forværringer i vinterhalvåret er vigtigt.
Astma patienter med allergi for husstøvmider oplever ofte forværring af astmasymptomerne i vinterhalvåret, hvor eksponering for miderne, pga. bedre vækstbetingelser, er størst. Sjældent opleves astmasymptomer udelukkende i vinterhalvåret, da ekspositionen for husstøvmider fortsætter over sommeren, dog oftest i mindre grad.
9.4. ALLERGEN IMMUNTERAPI (AIT)
AIT-behandling af astma patienter, subkutan immunterapi (SCIT) og sublingual immunterapi (SLIT), er bedst undersøgt hos patienter med mild astma. Hos patienter, hvis astma hovedsageligt er drevet af eksposition for allergener, her under astma patienter med allergisk rhinitis, har SCIT vist at reducere symptomer og medicin behov17, 18. SLIT-tabletter for husstøvmider kan formentlig reducere ICS dosis og forebygge eksacerbationer hos patienter med allergisk astma og hos patienter med både astma og allergisk rhinitis17,19. Af den årsag er AIT hyppigt relevant at overveje som behandlingstiltag ved patienter der ikke er velbehandlet for en allergisk astma.
SCIT-behandling kan tilbydes for en lang række allergener, mens SLIT behandling findes for træpollen(birkepollen)-, græspollen- og husstøvmideallergi. Mere information om AIT kan findes i Dansk Selskab for Allergologi’s vejledning: http://danskallergi.dk/wp-content/uploads/DSA-it-kliniske-retningslinier-final-260219.pdf
10. SÆRLIGE PATIENTGRUPPER
10.1. GRAVIDE
Gravide med astma skal i store træk behandles som alle andre astmatikere. Det vigtigste er at fastholde fokus på god astmakontrol og at astma-medicin som udgangspunkt kan anvendes uændret i graviditeten. I grove træk oplever 1/3 at få forbedring i deres astma under graviditeten, 1/3 mærker ingen ændring, og 1/3 oplever forværring under graviditeten. Ved anamneseoptagelse er det vigtigt at huske at flere almindelig forekommende tilstande hos den gravide kan være årsag til øget dyspnø: Øget tidalvolumen, faldende hæmoglobin, øget blodvolumen med heraf følgende forværring af eventuel nasalstenose, øget kropsvægt og især i tredje trimester betydeligt øget abdominalindhold.
Forekommer der eksacerbation af astmaen under graviditeten, er det vigtigt at starte relevant behandling mindst lige så hurtig som hos alle andre patienter med astma, også for at reducere risikoen for udvikling af hypoxi.
Gravide med astma skal tilbydes hyppigere opfølgning af deres astmabehandling. Ved manglende kontrol anbefales hurtig henvisning til lungemedicinsk vurdering.
ERS har nylig publiceret oversigtsartikel, hvori der findes oversigt over inhalationsmedicins indvirkning på graviditet og amning20.
10.2. PROFESSIONELLE SPORTSFOLK
Astma opstår hyppigere hos elite sportsfolk som dyrker endurance sport (35%) (svømning, roning, cykling) i forhold til f.eks. holdsport så som håndbold og fodbold. Når astmadiagnosen stilles, bør man overholde The International Olympic Committees (IOC) krav for diagnosen astma, af hensyn til elite sportsmandens muligheder for behandling uden risiko for doping mistanke. IOC kræver positiv objektiv test (reversibilitets test, metakolin, mannitol, hyperton NaCl eller EVH – men ikke PEF)21.
Hvert år udføres en liste over tilladte og forbudte stoffer. Listen findes på Anti-Doping Danmarks (ADD) (antidoping.dk) og på World Anti-Doping Agencys hjemmeside (wada-ama.org).
ICS og nasalsteroid er tilladt uden restriktioner. Der skal søges dispensation hos ADD for indtagelse af systemisk steroid mens det tages, men der er ikke karantæne efter kuren.
Følgende stoffer kan anvendes uden speciel dispensation (TUE ansøgning) enten et specifikt antal doser per dag, eller en specifik udskillelse i urinen ved dopingtest:
- Salbutamol max 8 * 0.1 microg/ds per 8 timer, med urin grænse på 1000 ng/mL)
- Formoterol under 54 microg/døgn
- Salmeterol under 100 microg * 2 per døgn
- Vilanterol max 25 microg/døgn
Terbutalin kræver TUE ansøgning til ADD.
Eliteatleter har ofte en fænotype som er præget af makrofager og ikke hverken eosinofile eller neutrofile granulocytter, hvorfor ICS ofte virker dårligere, klinisk erfaring er at det ofte kræver højere doseringer. Ved hyppig anvendelse af SABA opstår der takyfylaksi, med nedsat følsomhed for SABA således at der er langsommere indsættende effekt, det kræver flere doser for at opnå nær max effekt, og slutteligt opnås max FEV1 først efter yderligere indtagelse af SAMA eller LAMA. Dette er til stor gene for især elite idrætsudøvere der ved konkurrencer har behov for bedst mulig lungefunktion. Derfor foreslås det at de tager så begrænset mængde SABA og LABA som muligt. Takyfylaksi er ikke set ved brug af SAMA og LAMA. LAMA kræver, som reglerne er nu, ikke TUE ansøgning til ADD.
10.3. ERHVERVSBETINGET ASTMA
Mistænkes en patients astma at være forårsaget eller forværres af forhold på arbejdet skal patienten henvises til arbejdsmedicinsk vurdering.
11. PROGNOSE
11.1. REMISSION AF ASTMA
Astma er ikke nødvendigvis en livslang kronisk tilstand. Den inflammatoriske proces i luftvejene kan ophøre og sygdommen er herved helbredt. Hyppigheden hvormed det sker hos unge og voksne er ikke fuldt ud klarlagt. Fem års prognoses for remission af astma diagnosticeret i voksenalderen er formentlig kun på max 5%22, formentlig lavere. Remission blev defineret som minimum 12 måneder hvor patienten var medicinfri, symptomfri og uden tegn til astma (normal lungefunktion og FeNO). Heldigvis er prognosen betydelig bedre for børn og unge.
Følgende faktorer øger sandsynligheden for remission:
- Ung alder
- Tidlig debut af astma
- Atopi
- Allergisk rhinitis
- Få Ko-morbiditeter
Det er vigtigt at informerer patienterne om muligheden for fremtidig ny aktivitet i astmaen og ved tilbagefald af symptomerne skal de søge læge med henblik på vurdering og rettidig genoptagelse af astmabehandling.
11.2. RISIKO FOR VEDVARENDE LUFTVEJSOBSTRUKTION
De mest betydende faktorer, der øger risikoen for vedvarende luftvejsobstruktion hos patienter med astma er:
- Mangeårig manglende symptomkontrol
- Talrige eksacerbationer
- Rygning
- Mand
11.3. RISIKO FOR SVÆR EKSACERBATION OG DØD
Det er en misforstået antagelse, at patienter med mild og moderat astma ikke får svære eksacerbationer. I et ældre review er det estimeret af patienter med mild astma23, defineret som symptomer mindre end en gang per uge i de forudgående tre måneder, udgjorde:
- 30-40% af patienter med astmaforværringer vurderet på skadestue/i akutafdeling
- 16% af patienter med nær-fatale astma eksacerbationer
- 15-30% af patienter med fatalt forløbende eksacerbationer
Det er et af flere argumenter for, at SABA monoterapi ikke længere har plads i astma behandling, fordi SABA ikke forebygger eksacerbationer. Død af astma ses langt sjældnere end før udvikling af ICS, dog er der fortsat en diskret øget dødelighed blandt både unge og voksne.
12. REFERNENCER
1: T To, S Stanojevic, G Moores, AS Gershon, ED Bateman, AA Cruz and LP Boulet. Global asthma prevalence in adults: findings from the cross-sectional world health survey. BMC Public Health 2012; 12: 204.
2: S Suissa, P Ernst, JF Boivin, RI Horwitz, B Habbick, D Cockroft, L Blias et al. A cohort analysis of excess mortality in asthma and the use of inhaled beta-agonists. Am J Respir Crit Care Med 1994; 149: 604.
3: NH Gershman, HH Wong, JT Liu, JV Fahy. Low- and high-dose fluticasone propionate in asthma; effects during and after treatment. Eur Respir J 2000; 15: 11
4: AS Melani, M Bonavia, V Cilenti, C Cinti, M Lodi, P Martucci, M Serra et al.
Inhaler mishandling remains common in real life and is associated with reduced disease control, Respir Med 2011; 105(6): 930
5: R Beasley, J Harper, G Bird, I Maijers, M Weatherall and ID Pavord. Inhaled Corticosteroid Therapy in Adult Asthma Time for a New Therapeutic Dose Terminology. Am J Respir Crit Care Med 2019; 199(12): 1471
6: BF Chauhan and FM Ducharme. Addition to inhaled corticosteroids of long-acting beta2-agonists versus anti-leukotrienes for chronic asthma (Review). Cochrane Database of Systematic Reviews 2014; 1
7: H Mosbech, R Deckelmann, F Blay, MD, EA Pastorello, E Trebas-Pietras, LP Andres, I Malcus et.al. Standardized quality (SQ) house dust mite sublingual immunotherapy tablet (ALK) reduces inhaled corticosteroid use while maintaining asthma control: A randomized, double-blind, placebo-controlled trial. J Allergy Clin Immunol 2014; 134: 568
8: BF Chauhan BF and FM Ducharme. Anti-leukotriene agents compared to inhaled corticosteroids in the management of recurrent and/or chronic asthma in adults and children. Cochrane Database Syst Rev 2012; 5
9: DM Sobieraj, WL Baker, E Nguyen, ER Weeda, CI Coleman, CM White, SC Lazarus et al. Association of Inhaled Corticosteroids and Long-Acting Muscarinic Antagonists with Asthma Control in Patients With Uncontrolled, Persistent Asthma A Systematic Review and Meta-analysis. JAMA 2018; 319(14): 1473
10: CJ Cates, BH Rowe. Vaccines for preventing influenza in people with asthma. Cochrane Database Syst Rev 2013; 2
11: E Vasileiou, A Sheikh, C Butler, K El Ferkh, B von Wissmann, J McMenamin, L Ritchie et al. Effectiveness of Influenza Vaccines in Asthma: A Systematic Review and Meta-Analysis. Clin Infect Dis 2017; 65
12: B Stenius-Aarniala, T Poussa, J Kvarnström, EL Grönlund, M Ylikahri, P Mustajoki. Immediate and long term effects of weight reduction in obese people with asthma: randomised controlled study. BMJ 2000; 320: 827
13: FB Adeniyi, T Young. Weight loss interventions for chronic asthma. Cochrane Database Syst Rev 2012; 7
14: ESH Hansen, A Pitzner-Fabricius, LL Toennesen, HK Rasmusen, M Hostrup, Y Hellsten, V Backer et al.
Effect of aerobic exercise training on asthma in adults: a systematic review and meta-analysis. Eur Respir J 2020: 30; 56
15: JB Hagan, SA Samant, GW Volcheck, JT Li, CR Hagan, PJ Erwin, MA Rank. The risk of asthma exacerbation after reducing inhaled corticosteroids: a systematic review and meta-analysis of randomized controlled trials. Allergy 2014; 69: 510
16: T Shirai, T Matsui, K Suzuki, K Chida. Effect of pet removal on pet allergic asthma. Chest 2005; 127: 1565
17: I Agache, S Lau, CA Akdis, S Smolinska, M Bonini, O Cavkaytar, B Flood et al. EAACI Guidelines on Allergen Immunotherapy: House dust mite-driven allergic asthma. Allergy 2019; 74: 855
18: MJ Abramson, RM Puy, JM Weiner. Injection allergen immunotherapy for asthma. Cochrane Database Syst Rev 2010; 8
19: JC Virchow, V Backer, P Kuna, L Prieto, H Nolte. Efficacy of a House Dust Mite Sublingual Allergen Immunotherapy Tablet in Adults With Allergic Asthma A Randomized Clinical Trial. JAMA 2016; 315(16): 1715
20: PG Middleton, EJ Gade, C Aguilera, L MacKillop, BM Button, C Coleman, B Johnson, V Bacher et al. ERS/TSANZ Task Force Statement on the management of reproduction and pregnancy in women with airways diseases. Eur Respir J 2020; 55: 1901208
21: The International Olympic committee. IOC Consensus Statement on Asthma in Elite Athletes January 2008. Olympic.org
22: LE Tuomisto, P Ilmarinen, H Kankaanranta. Prognosis of new-onset asthma diagnosed at adult age. Respir Med 2015; 109: 944
23: D Dusser, D Montani, P Chanez, J de Blic, C Delacourt, A Deschildre, PDevillier, et al. Mild asthma: an expert review on epidemiology, clinical characteristics and treatment recommendations. Allergy 2007; 62: 591