1.0. GENERELT
Lungevolumenreduktion (LVR) til behandling af hyperinflation ved emfysem omfatter lungevolumen reducerende kirurgi (LVRK) og bronkoskopisk lungevolumen reduktion (BLVR). Begge er evidente behandlingsmodaliteter i GOLD guidelines (evidens A) samt i NICE til selekterede patienter1.
1.1. Baggrund
Hos KOL-patienter med emfysem er hyperinflationen en væsentlig årsag til symptombyrden, særligt i form af åndenød ved aktivitet. Patienterne har et øget residualvolumen med heraf nedsat bevægelighed af diafragma2, et nedsat diastolisk fyldningstryk, som betinger nedsat venstre ventrikelfunktion3, og dermed flere faktorer der til sammen giver øget dyspnø.
Behandlingen af emfysem er baseret på at reducere hyperinflationen. Dette gælder for den medicinske bronkodilaterende behandling men yderligere reduktion kan foregå med enten kirurgisk teknik eller som bronkoskopisk procedure. Formålet med LVR er at reducere symptombyrden, bedre funktionsniveau og lungefunktion samt potentielt forbedre overlevelsen4,5.
2.0. UDREDNING
Den primære udredning er rettet mod at vurdere graden af hyperinflation som årsag til patientens dyspnø samt udelukke konkurrerende årsager til dyspnø som f.eks. hjertesvigt, arytmi og dekonditionering. Dette kan foregå på alle lungemedicinske afdelinger. Vurdering af den endelige behandlingsindikation er en højtspecialiseret funktion, som varetages på de højtspecialiserede lungemedicinske afdelinger. I Danmark drejer det sig om universitetshospitalerne i Aalborg, Odense, Aarhus samt Rigshospitalet. Her vurderer et multidisciplinært team (MDT) ved konference den endelige behandlings indikation og afgør, hvordan behandlingen bedst foretages for at opnå det bedste resultat.
For tiden foretages LVRK kun på Rigshospitalet. Patienter der ikke er kandidater til BLVR eller ikke ønsker denne behandling, men vil have gavn af LVR, kan således via MDT-konference henvises til Rigshospitalet mhp. LVRK.
2.1. Initialt udredningsprogram
Før henvisning til LVR skal patienten være optimalt medicinsk behandlet og have gennemgået et rehabiliteringsprogram og være fysisk aktiv til daglig. Det indledende udredningsprogram består både af anamnestiske oplysninger, biokemiske analyser, billeddiagnostiske undersøgelser samt fysiologiske undersøgelser af lunger og hjerte. Se desuden Figur 1.
Tabel 1. Kriterier for LVR
| Alder | 40-75 år |
| BMI | 18-30 (anbefalet) |
| Tobak | Ophør > 6 mdr. |
| MRC | ≥ 3 |
| 6MWT | ≥140-500 m* |
| FEV1 | 20-45% |
| TLC | > 100% |
| RV | > 175% |
| RV/TLC | > 58% |
| DLCO | > 20% |
| HRCT | Ingen uafklarede infiltrater,
hvor malignitet ikke kan udelukkes på CT thorax indenfor 6 mdr. |
| pCO2 | < 7,5 kPa |
| pO2 | > 6 kPa |
| EKKO | TR-gradient < 40 mmHg |
| Diverse | Gennemført KOL rehabilitering forud for udredning. |
*Ved 6MWT > 4-500 m må det vurderes, om symptombyrden er stor nok til at opnå fordele ved LVR.
Tabel 2. Kontraindikationer for LVR
| Tobak | Rygning de seneste 6 måneder |
| Thorax | Svære thorakale deformiteter og nogle tidligere lungeoperationer |
| Pleura | Udbredte forandringer/sequelae. efter tidligere pleurodese eller empyem |
| Reversibilitet | Forbedring af FEV1 > 12% eller 200 mL |
| Prednisolon | >10 mg dagligt |
| Symptomer | Bronkiektasier eller kronisk slimproducerende bronkit, der ikke kan saneres |
| Komorbiditet | Svær iskæmisk hjertesygdom (individuel vurdering), pulmonal hypertension, malign sygdom, dialysekrævende nyreinsufficiens, levercirrose eller anden alvorlig konkurrerende sygdom |
2.1.1. Anamnestiske oplysninger
Graden af dyspnø (MRC score), symptombyrde (CAT score) og tidligere rehabilitering noteres. Tilstedeværelsen af kronisk bronkitis fastlægges (kontraindikation for LVR grundet risiko for efterfølgende infektion, tillukning af ventiler, samt manglende effekt af behandlingen), hvilket defineres som daglig hoste med betydende opspyt (kan forsøges saneret inden der tages stilling til LVR).
Forud for LVR skal patienten have været røgfri i mindst 6 måneder, da fortsat tobaksrygning kan være årsag til vedvarende symptomer samt øge risikoen for infektioner, ligesom rygestop kan virke lindrende i sig selv.
Alle patienter bør gennemgå rehabilitering og optimering af den medicinske behandling før henvisning til LVR.
2.1.2. Helkropspletysmografi og DLCO
Udføres efter almindeligt gældende retningslinjer. Se Tabel 1 for grænseværdier.
2.1.3. Arteriepunktur
Arteriepunktur udføres uden ilt. Se Tabel 1 for grænseværdier.
2.1.4. Alder
Hverken høj eller lav alder er en absolut kontraindikation for LVR, men alder mellem 45-75 år bør tilstræbes. Ved lav alder bør anden ætiologi til symptomer overvejes og α1-antitrypsin(A1AT)-mangel skal udredes.
2.1.5. BMI
Der tilstræbes et BMI mellem 18 – 30 uanset type af LVR. Lavere BMI er associeret med øget risiko for komplikationer og længere indlæggelses-varighed6,7 ved både LVRK og BLVR. Højere BMI kan i sig selv være en modificerbar årsag til dyspnø, men øger også risikoen for komplikationer i efterforløbet af LVR.
2.1.6. 6 minutters gangtest (6MWT)
Det er vigtigt at patienten forud for LVR har potentiale for at kunne opnå et bedret funktionsniveau efter indgrebet. Dette vurderes ved 6MWT, hvormed man kan vurdere patients aktuelle funktionsniveau, dyspnø grad og om patienten er dekonditioneret. Således har man på baggrund af ekspert-konsensus vurderet, at 6MWT skal være over 140 meter8,9. Der er ingen formelle øvre grænser, men hvis over 4-500 meter synes den potentielle gevinst ved indgrebet beskeden i forhold til risici.
2.1.7. HRCT
Som en del af udredningsprogrammet udføres HRCT i 3 plan i in- og ekspiration mhp. at vurdere emfysemgrad/fordeling (Heterogent/Homogent) samt udelukke malignitetssuspekte infiltrater, bronkiektasier, sekretstagnation eller betydende luftvejskollaps ((EDAC) Ekspiratory Dynamic Airway Colapse).
På de specialiserede centre anvendes scanningen også til at bestemme komplethed af fissur, hvis der skal udføres BLVR samt bestemme hvilken lap, der er mest egnet til aflukning eller fjernelse. Fissurernes komplethed i forhold til target-lappen kan bestemmes før og/eller under indgrebet (se afsnit 2.1.10).
2.1.8. Ekkokardiografi og EKG
Elektrokardiogram (EKG) udføres for at udelukke arytmi eller tegn på iskæmisk hjertesygdom, som begge kan være medvirkende til dyspnø og også udgør en risikofaktor eller kontraindikation ved LVR.
Ekkokardiografi skal udføres primært med henblik på at udelukke hjertesvigt eller klapsygdom som årsag til dyspnø, samt vurdere eventuel sekundær pulmonal hypertension (PH). Hvis der findes PH med trikuspidal returgradient over 40 mmHg vil dette udgøre en konkurrerende årsag til dyspnø samt en risikofaktor ved indgrebet og derfor være en kontraindikation for LVR.
2.1.9. Perfusionsscintigrafi
Kan udføres til at støtte udvælgelse af den bedst egnede lungelap til behandlingen, specielt mht. diversitet i perfusionen. Vurderingen optimeres ved supplerende ventilationsscintigrafi, og er bedst hvis udført som V/Q SPECT/CT14.
2.1.10. Undersøgelse af fissurens integritet
Fissur komplethed (kollateral ventilation) kan vurderes på forskellig vis.
- HRCT i 3 plan med både in- og ekspirationsoptagelse
- Kommercielt tilgængelige softwaresystemer til efterbehandling af CT-scanninger kan anvendes til at vurdere emfysemgrad, volumen og i nogle tilfælde fissurernes komplethed
- Chartis® kan teste fissurens integritet definitivt ved intraoperativt at lukke den udvalgte lap. Evt. returflow fra fissuren registreres via et analysesystem
Ved inkomplette fissurer vil BLVR med ventiler være kontraindiceret i den pågældende lap da der sandsynligvis ikke vil være effekt, men derimod en betydelig risiko for komplikationer.
2.2. Samlet vurdering efter udredning
Det samlede udredningsprogram vurderes ved MDT med deltagelse af bl.a. thoraxkirurg, radiolog, klinisk fysiolog og lungemedicinsk speciallæge.
Her besluttes det om LVR er en egnet behandling til patienten og hvilken metode der med højest sandsynlighed vil føre til et godt resultat for den enkelte patient.
3.0. LVRK
3.1. Baggrund
LVRK var primært indiceret til patienter med apikalt lokaliseret emfysem. Nyere serier viser dog at LVRK også er brugbart til andre områder af lungen inkl. homogent emfysem og A1AT-mangel. I modsætning til BLVR er LVRK ikke afhængig af intakte fissurer og lokalisering i en enkelt lap, men kan skræddersys til emfysemfordelingen hos den enkelte patient. Indgrebet foregår oftest som video-assisteret thorakoskopisk kirurgi (Video Assisted Thoracic Surgery (VATS)). Der kan i samme seance foretages både unilateralt eller bilateralt indgreb, men i Danmark anvendes oftest et unilateral indgreb15
3.2. Effekt
Sammenlignet med konservativ behandling kan LVRK reducere mortaliteten årligt med 50% hos patienter med overlapsemfysem og lav fysisk kapacitet16. Hos patienter med anden fordeling af emfysem ses i ældre opgørelser en øget tendens til mortalitet 2 år efter LVRK. Den bedste effekt opnås typisk ved lokaliseret overlapsemfysem med forbedring i livskvalitet og fysisk kapacitet efter 2 år16. En forbedring af FEV1 på mindst 10% ses hos omkring 50% af patienterne efter 12 måneder, en forbedring i 6MWT ses hos 41% og bedring i subjektiv følelse af åndenød hos ca. 60%17. Da der også er patienter, der slet ikke oplever effekt eller oplever komplikationer, er det vigtigt med grundig information forud for patientens beslutning.
Patienter med heterogent emfysem har betydeligt bedre behandlingsrespons, end hvis emfysemet er homogent fordelt10. Behandling af homogent emfysem er mulig både med BLVR og LVRK, men den samlede effekt er typisk mindre end ved heterogent emfysem. Dette skyldes at indgrebet medfører tab af diffusion, som skal opvejes af bedret ventilation10–13
3.3. Komplikationer
Tabel 3. Vigtigste komplikationer til LVRK
| Luftlækage | Den hyppigste komplikation. De fleste (≈ 90%) oplever nogen grad af luftlækage uden behov for intervention, mens omkring 10% behøver re-operation |
| Død | 90 dages mortaliteten er ca. 7,9%16 |
| Pneumoni | 30-dages incidens 14%17 |
| Arytmier | Hyppigst AFLI/AFLA, forekommer hos ca. 20% 30 dage postoperativt17 |
| Andre (ved VATS) | Urinretention (2%), lungeemboli (1-2%), sepsis (4%)17 |
4.0. BLVR
4.1. Baggrund
Ved BLVR indsættes en-vejs-ventiler via bronkoskop i bronkiesystemet med henblik på at opnå komplet aflukning af en lap og derved en atelektase, hvorved der opnås volumenreduktion.
En af fordelene ved anvendelsen af BLVR er, at proceduren er reversibel, og ventilerne kan fjernes igen i tilfælde af komplikationer.
Forventet postoperativ indlæggelsesvarighed er mindst 2 dage pga. risikoen for pneumothorax.
4.2. Effekt
Subjektiv bedring i åndenød ses hos 50-60% af patienterne i løbet af de første 6-12 måneder. Bedring i FEV1 indenfor 12 måneder på mindst 12% ses hos ca. 60%, og mindst 15% bedring ses hos 37-48%.
Forbedring i 6MWT på ≥25 m ses hos 30-50% i løbet af de første 12 måneder.
Effekten er afhængig af dannelsen af atelektase, og hos de patienter, hvor atelektase dannes, ses en markant større effekt.
Hos patienter, der ikke opnår effekt eller har komplikationer, kan ventilerne fjernes eller omlægges ved gentaget bronkoskopi
Efter BLRV vil de patienter, der oplever effekt, have en betydeligt bedre livskvalitet, men da der også er omkring 1/3 af patienterne, der ikke oplever effekt og/eller i stedet komplikationer, er grundig information forud for patientens beslutning vigtig 18–20.
Udførelse af BLVR udelukker ikke senere LVRK.21
4.3. Komplikationer
Tabel 4. Vigtigste komplikationer til BLVR
| Pneumothorax | Den hyppigste og alvorligste komplikation. 30-dages-prævalensen er rapporteret omkring 20%19,22,23 |
| Død | Mortaliteten varierer imellem studier, men 30-dages mortalitet er 1-3%19,20,22, hvoraf nogle studier ikke oplever procedure-relaterede dødsfald. |
| Pneumoni og anden lunge-infektion | 30-dages prævalens på 1-5%19,20,22,23 |
| KOL exacerbation | Varierer meget mellem studierne, men 30-dages-prævalensen er ikke signifikant højere end for en kontrolgruppe19,20 |
| Hæmoptyse | 30-dages prævalens: ca. 2%19,20,22 |
| Ophostning af ventiler | Forekommer hos 0-2% af alle der får foretaget BLVR22,23. |
| Fjernelse/
Genanlæggelse /oprensning af ventiler |
Hyppigste årsager pneumothorax, forværring af åndenød, dannelse af granulationsvæv eller infektion. Foretages hos 20-30% af patienterne indenfor 6 måneder20,22,23 |
5.0. EFTERBEHANDLING OG KONTROL
Patienterne kontrolleres typisk efter LVR for at vurdere behandlingseffekten. Dette kan være forskelligt afhængigt af lokale programmer. Typisk ses patienterne efter 1, 3, 12 og 24 måneder. Et kontrolbesøg kan bestå af udvidet LFU med diffusionsmåling og helkropspletysmografi, 6MWT og røntgen af thorax.
Patienterne tilrådes at anvende effekten af den lindrende behandling til at opnå bedre fysisk formåen eventuelt igennem et rehabiliteringsprogram eller på eget initiativ.
6.0. ANDRE BEHANDLINGSMETODER
Der har været eksperimenteret med andre måder at foretage bronkoskopisk lungevolumen reduktion som f.eks. Lung Volume Reduction Coils (LVRC®), to- komponent polymergel, vanddamp, etc. Fælles for dem alle er, at der har været varierende grader af effekt og bivirkninger. Ingen af modaliteterne er til dato lige så gennemprøvede som dem, der er beskrevet ovenfor. Derfor er disse behandlinger for øjeblikket heller ikke tilgængelige udenfor studieprotokoller.
7.0. LUNGETRANSPLANTATION
Lungetransplantation er den ultimative behandling af emfysem (se specifik DLS retningslinje).
Metoden indebærer udfordringer i forhold til operationens risikoprofil, den typiske patients alder og komorbiditeter samt lavt udbud af donorlunger.
Forudgående LVRK eller BLVR er ikke en kontraindikation for senere lungetransplantation.
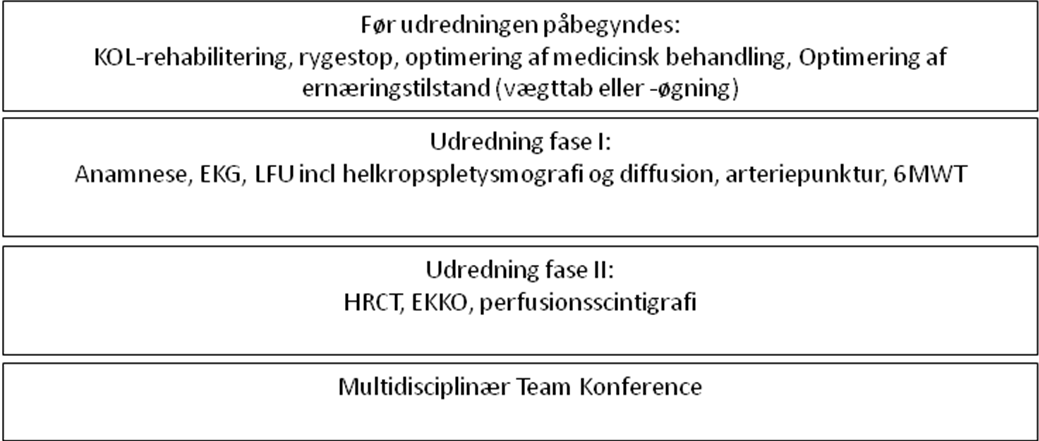
Figur 1 Simplificeret opsummering af forløb og udredning til lungevolumenreduktion (LVR). Hvis de i fase I angivne undersøgelser opfylder kravene, fortsættes til fase II, hvorefter patienten vurderes på MDT konference og vurderes enten uegnet eller egnet til lungevolumenreducerende kirurgi eller endobronkiale ventiler.
REFERENCER
- GOLD COMMITTEE. 2021 GLOBAL STRATEGY FOR PREVENTION, DIAGNOSIS AND MANAGEMENT OF COPD. 2021:12-19. https://goldcopd.org/wp-content/uploads/2020/11/GOLD-REPORT-2021-v1.1-25Nov20_WMV.pdf.
- Dos Santos Yamaguti WP, Paulin E, Shibao S, et al. Air trapping: The major factor limiting diaphragm mobility in chronic obstructive pulmonary disease patients. Respirology. 2008. doi:10.1111/j.1440-1843.2007.01194.x
- Alter P, Watz H, Kahnert K, et al. Airway obstruction and lung hyperinflation in COPD are linked to an impaired left ventricular diastolic filling. Respir Med. 2018. doi:10.1016/j.rmed.2018.02.011
- Garner J, Kemp S V, Toma TP, et al. Survival after Endobronchial Valve Placement for Emphysema: A 10-Year Follow-up Study. Am J Respir Crit Care Med. 2016;194(4):519-521. doi:10.1164/rccm.201604-0852LE
- Naunheim KS, Wood DE, Mohsenifar Z, et al. Long-term follow-up of patients receiving lung-volume-reduction surgery versus medical therapy for severe emphysema by the National Emphysema Treatment Trial Research Group. Ann Thorac Surg. 2006;82(2):431-443. doi:10.1016/j.athoracsur.2006.05.069
- Fernandez-Bussy S, Kornafeld A, Labarca G, Abia-Trujillo D, Patel NM, Herth FJF. Endoscopic Lung Volume Reduction in Relation to Body Mass Index in Patients with Severe Heterogeneous Emphysema. Respiration. 2020;99(6):477-483. doi:10.1159/000507591
- Vaughan P, Oey IF, Steiner MC, Morgan MDL, Waller DA. A prospective analysis of the inter-relationship between lung volume reduction surgery and body mass index. Eur J cardio-thoracic Surg Off J Eur Assoc Cardio-thoracic Surg. 2007;32(6):839-842. doi:10.1016/j.ejcts.2007.09.016
- Herth FJF, Slebos D-J, Criner GJ, Valipour A, Sciurba F, Shah PL. Endoscopic Lung Volume Reduction: An Expert Panel Recommendation – Update 2019. Respiration. 2019;97(6):548-557. doi:10.1159/000496122
- Slebos D-J, Shah PL, Herth FJF, Valipour A. Endobronchial Valves for Endoscopic Lung Volume Reduction: Best Practice Recommendations from Expert Panel on Endoscopic Lung Volume Reduction. Respiration. 2017;93(2):138-150. doi:10.1159/000453588
- Sciurba FC, Ernst A, Herth FJF, et al. A randomized study of endobronchial valves for advanced emphysema. N Engl J Med. 2010;363(13):1233-1244. doi:10.1056/NEJMoa0900928
- Valipour A, Slebos D-J, Herth F, et al. Endobronchial Valve Therapy in Patients with Homogeneous Emphysema. Results from the IMPACT Study. Am J Respir Crit Care Med. 2016;194(9):1073-1082. doi:10.1164/rccm.201607-1383OC
- Klooster K, Ten Hacken NHT, Franz I, Kerstjens HAM, van Rikxoort EM, Slebos D-J. Lung volume reduction coil treatment in chronic obstructive pulmonary disease patients with homogeneous emphysema: a prospective feasibility trial. Respiration. 2014;88(2):116-125. doi:10.1159/000362522
- Caviezel C, Schneiter D, Opitz I, Weder W. Lung volume reduction surgery beyond the NETT selection criteria. J Thorac Dis. 2018;10(Suppl 23):S2748-S2753. doi:10.21037/jtd.2018.08.93
- Kristiansen JF, Perch M, Iversen M, Krakauer M, Mortensen J. Lobar Quantification by Ventilation/Perfusion SPECT/CT in Patients with Severe Emphysema Undergoing Lung Volume Reduction with Endobronchial Valves. Respiration. 2019;98(3):230-238. doi:10.1159/000500407
- Nodin E, Hansen HJ, Ravn J, Perch M. Kirurgisk lungevolumenreduktion til behandling af svært emfysem. Ugeskr Laeger. 2019:2-5.
- Fishman A, Martinez F, Naunheim K, et al. A randomized trial comparing lung-volume-reduction surgery with medical therapy for severe emphysema. N Engl J Med. 2003;348(21):2059-2073. doi:10.1056/NEJMoa030287
- McKenna RJJ, Benditt JO, DeCamp M, et al. Safety and efficacy of median sternotomy versus video-assisted thoracic surgery for lung volume reduction surgery. J Thorac Cardiovasc Surg. 2004;127(5):1350-1360. doi:10.1016/j.jtcvs.2003.11.025
- Criner GJ, Delage A, Voelker K, et al. Improving Lung Function in Severe Heterogenous Emphysema with the Spiration Valve System (EMPROVE). A Multicenter, Open-Label Randomized Controlled Clinical Trial. Am J Respir Crit Care Med. 2019;200(11):1354-1362. doi:10.1164/rccm.201902-0383OC
- Kemp S V, Slebos D-J, Kirk A, et al. A Multicenter Randomized Controlled Trial of Zephyr Endobronchial Valve Treatment in Heterogeneous Emphysema (TRANSFORM). Am J Respir Crit Care Med. 2017;196(12):1535-1543. doi:10.1164/rccm.201707-1327OC
- Criner GJ, Sue R, Wright S, et al. A Multicenter Randomized Controlled Trial of Zephyr Endobronchial Valve Treatment in Heterogeneous Emphysema (LIBERATE). Am J Respir Crit Care Med. 2018;198(9):1151-1164. doi:10.1164/rccm.201803-0590OC
- Caviezel C, Guglielmetti L-C, Ladan M, et al. Lung volume reduction surgery as salvage procedure after previous use of endobronchial valves. Interact Cardiovasc Thorac Surg. 2021;32(2):263-269. doi:10.1093/icvts/ivaa261
- Fiorelli A, D’Andrilli A, Bezzi M, et al. Complications related to endoscopic lung volume reduction for emphysema with endobronchial valves: results of a multicenter study. J Thorac Dis. 2018;10(Suppl 27):S3315-S3325. doi:10.21037/jtd.2018.06.69
- Klooster K, ten Hacken NHT, Hartman JE, Kerstjens HAM, van Rikxoort EM, Slebos D-J. Endobronchial Valves for Emphysema without Interlobar Collateral Ventilation. N Engl J Med. 2015;373(24):2325-2335. doi:10.1056/NEJMoa1507807